治療戦略と長期予後観察の一例
SFA起始部のランディングに悩むCTO病変に対しゴア® バイアバーン® ステントグラフトを用いてEVTを完遂し、2年経過を観察した一例
はじめに
末梢動脈疾患(PAD)における最も病変頻度の高い大腿膝窩動脈領域において、長区間病変は血管内治療(EVT)の大きな問題点の一つである。デバイスの開発や手技の向上により初期成功率は非常に高くなったものの、血行再建後の開存率に関しては現在も解決されていない問題点として挙げられる。
ゴア® バイアバーン® ステントグラフトは発売より 3年以上が経過し、Japan IDE試験では平均病変長 21.8 cmの長区間病変に対し使用され、1年の一次開存率が 88.1%、2・3・4・5 年のTLR回避率がそれぞれ 87.2%・86.0%・83.4%・79.1% と長期においても良好な成績であることが報告されている。1
ただし、良好な成績を得るために病変をフルカバーすることの重要性が発売当初より推奨されており、今回SFA起始部にプラークを伴う閉塞病変に対しバイアバーン® ステントグラフトを用いてEVTを行った症例を提示する。

患者背景・病変背景
- 年齢 : 80代
- 性別 : 男性
- リスク因子 : 高血圧症,過去の喫煙歴
- Rutherford 分類 : Class 3
- 治療前 ABI : 右 1.13/ 左 0.67
- 対象病変部位(図1): 左 SFA 閉塞(病変長約22 cm)
- TASC Ⅱ 分類 : D
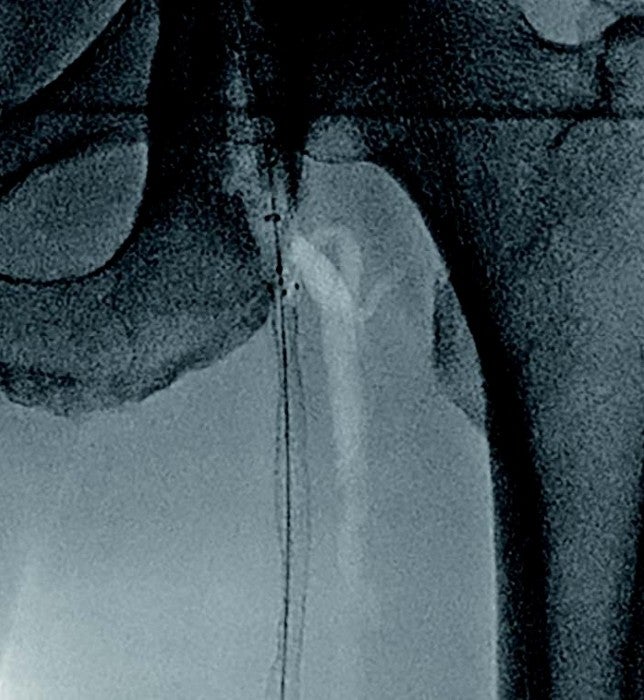
図1:術前
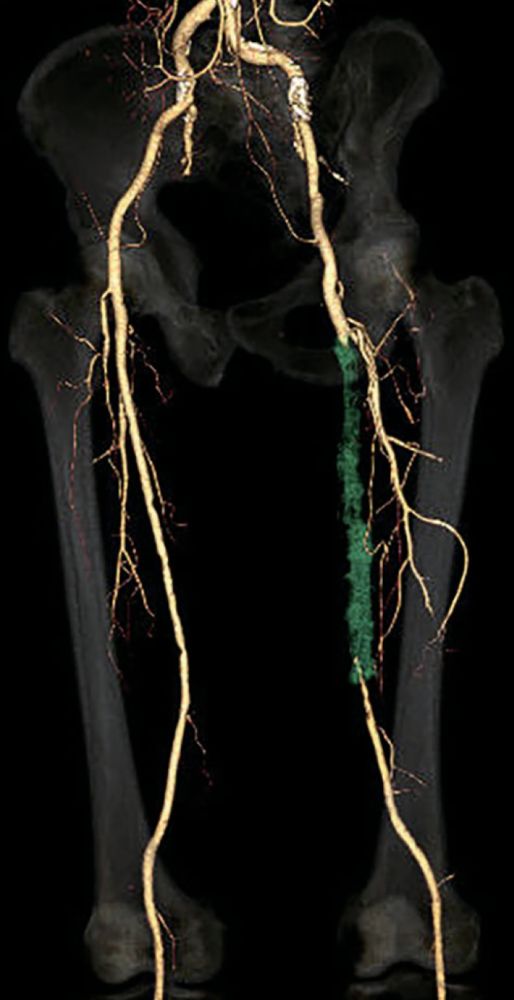
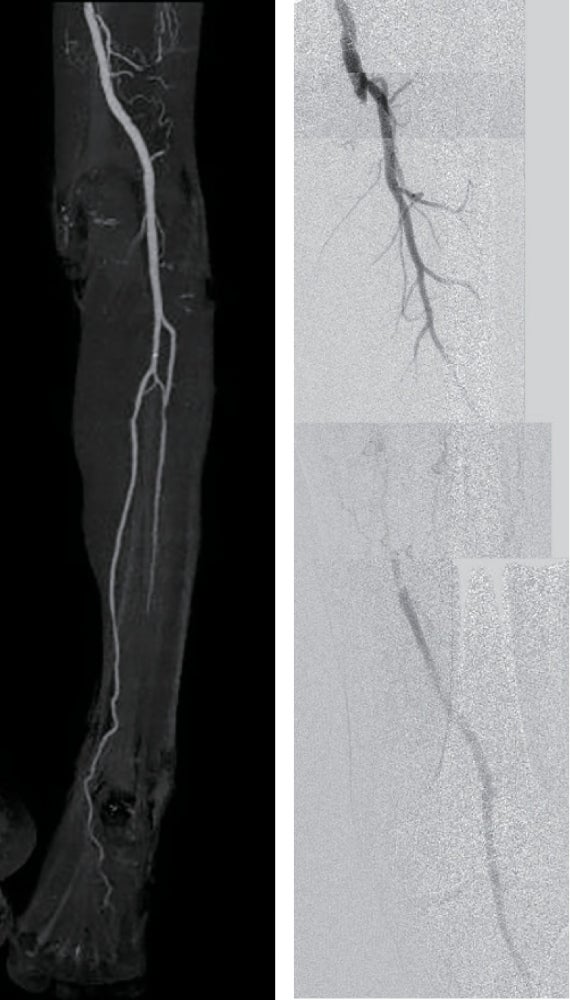
治療戦略
右CFA穿刺によるcontralateral approachにてdirect IVUS crossingおよび IVUSガイドにantegrade wiringを行い、sub-intimal trackingであれば distal punctureによるbi-directional approachを構築。病変長が20 cm長超えのため DCBは適応外であることから、拡張良好であればPOBAのみにて終了し、不良であれば scaffoldを追加することとした。
手技内容
- 右CFAを穿刺し、6 Fr. ガイディングシース(90 cm長)を4 Fr. JL1.0 造影カテ+0.035 inchガイドワイヤー(先端形状1.5 mm-J)を用いて cross-over。
※筆者は、SFA-CTOの場合に、IVUS でintra-plaqueであることが確認できた部位までガイディングシースを挿入することが多いため、比較的長いガイディングシースを選択している。 - IVUSをバックアップに0.014 inchガイドワイヤーにてantegrade wiringを開始したが、すぐにsub-intimalへ迷入したことからIVUSガイドにCTO用0.014 inchテーパードガイドワイヤーにてintra-plaqueへwiring。
- direct IVUS crossingとIVUS guidance wiringを繰り返すが、中途でintra-plaqueへ戻すことが困難となった。
- frontal pop.A. puncture(OMOTE Hiza-pun.)を行い、0.014 inchガイドワイヤー → マイクロカテーテルを挿入。
- 閉塞近位部でCTO用0.014 inchテーパードガイドワイヤー にて6 Fr. ガイディングシース内への rendez-vousに成功。
- 6 Fr. ガイディングシース内でマイクロカテーテルへ再度rendez-vousを行いexternalization。
- IVUSにてほぼ全てintra-plaque wiringであることを確認し、径4.0/長150 mmセミコンバルーンにて拡張。
- 径6.0/長150 mm高圧バルーンにて追加拡張したが血流改善に乏しく、BTK は良好なone straight lineが確保されていたことからバイアバーン® ステントグラフトを留置することとした。
- IVUSにて遠位部のヘルシーな部分をマーキングし、バイアバーン® ステントグラフト径6.0/長250 mm を留置(図2)。
- 径6.0/長150 mm高圧バルーンにてP3 segmentの穿刺部止血を兼ね長時間拡張し、バイアバーン® ステントグラフト内を高圧拡張。
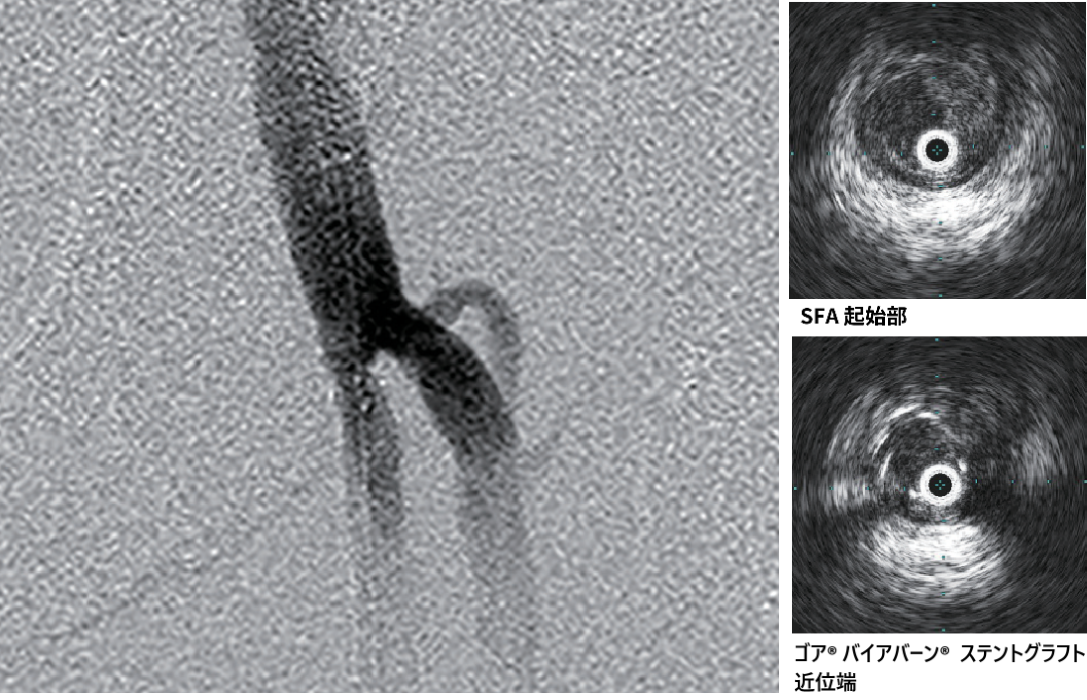
- 造影上は良好な血流改善を得られたが、IVUSではSFA起始部にプラーク残存を認めた(図3)。
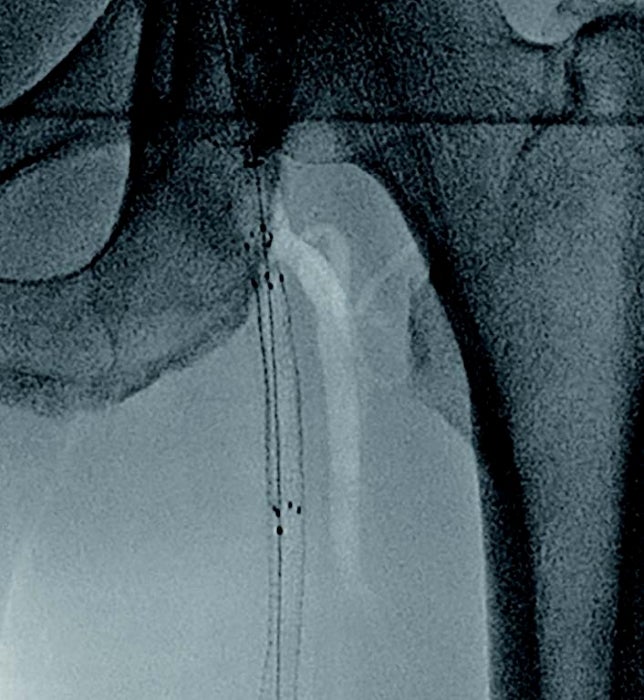
- プラークをフルカバーするため、SFA起始部にバイアバーン® ステントグラフト径6.0/長50 mmを追加留置(図4)。
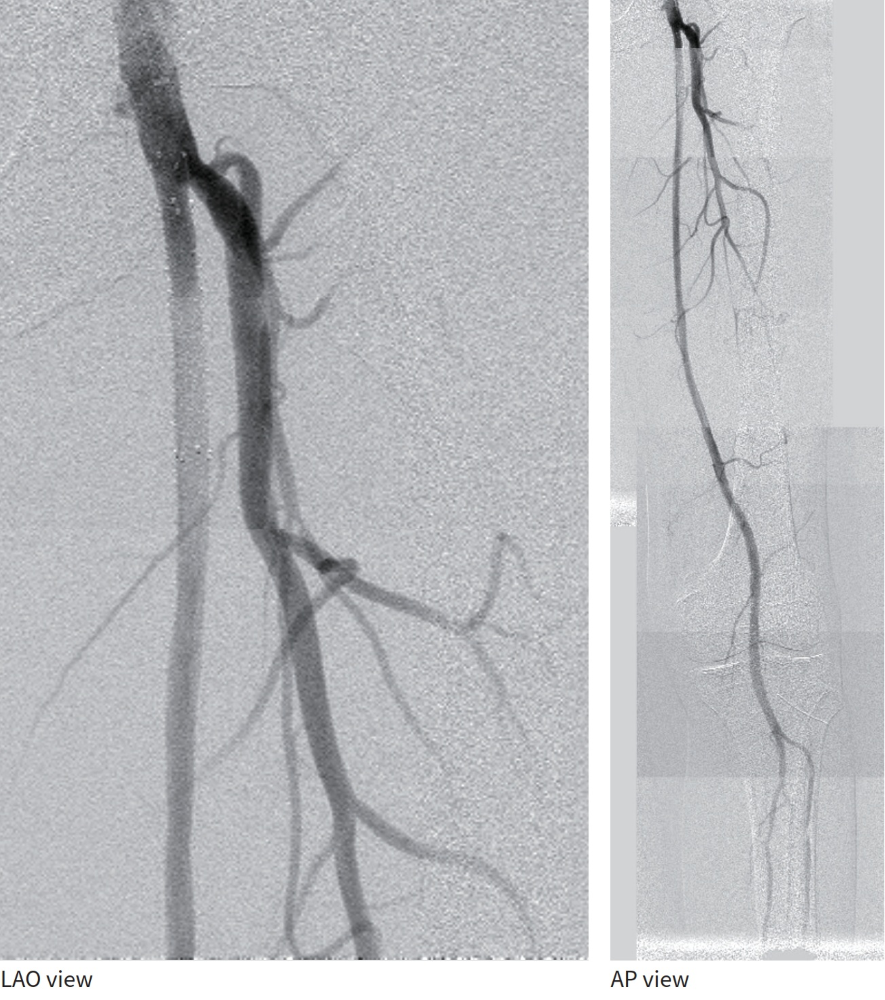
- 径6.0/長150 mm高圧バルーンにて高圧拡張を追加し、DFAの血流も問題がないことを確認して手技終了(図5)。
使用デバイス
- ガイディングシース:6 Fr.,長さ90 cm
- ガイドワイヤー:
- 0.014 inch,長さ300 cm 1本
- 0.014 inch,長さ190 cm(CTO 用テーパード)1本
- マイクロカテーテル:長さ60 cm
- ステント:
- バイアバーン® ステントグラフト 径6.0/長250 mm 1本
- バイアバーン® ステントグラフト 径6.0/長50 mm 1本
- バルーン:
- 径4.0/長150 mm セミコンバルーン 1本
- 径6.0/長150 mm 高圧バルーン 1本
- IVUS
治療のポイント
SFAの長区間病変でBTKに少なくとも良好なone straight lineが確保されていること、「distal」 にランディングゾーンが有されていること、6.0 mm以上のバイアバーン® ステントグラフト留置が可能な血管径であること、以上全てを満たす場合のscaffoldとしてバイアバーン® ステントグラフトは長期的に高い開存率を期待できると考える。
臨床経過
| <左 ABI > | |||||
|---|---|---|---|---|---|
| EVT 前 | 0.67 | 6か月後 | 1.19 | 18か月後 | 1.10 |
| EVT 翌日 | 1.23 | 12か月後 | 1.20 | 24か月後 | 1.18 |
| 1か月後 | 1.17 |
他院でシロスタゾールを開始され保存的経過観察となっていた症例で、Class 2–3の間欠性跛行残存に対する積極的治療希望にてEVTを行ったが、EVT後2年以上を経過した現在まで良好な経過を辿っている。
最後に
今回、バイアバーン® ステントグラフトを用いてSFA起始部のランディングに悩むCTO病変に対する EVTを報告させていただいた。現在、SFAに対するEVTのfinalized deviceが多数あり、術者として選択に困られている先生方も少なくないと思われる。筆者自身は、DCB発売前よりCTOでもPOBA のみで終了していたことも多く、現在でも可能な限りscaffoldを避けるよう手技を行っている(そのためにはintra-plaque wiringが重要であると考える)。しかし、実際にはscaffoldを必要とする病変が少なからずあり、その際に「治療のポイント」で記載した条件を満たしている場合には積極的にバイアバーン® ステントグラフトを選択している。
また、バイアバーン® ステントグラフト留置後の閉塞に対する懸念に関して、留置条件を満たした場合の開存率および閉塞率の成績は過去のデータで示されている。2
あらゆるデバイスに共通することではあるが、デバイスの特性を理解し、最大限の効果を発揮できるよう使用することも我々interventionalistが有するべき技量の一つであると筆者は考える。
治療前後の造影動画
- Yamaoka T, VIABAHN the latest real world clinical data from Japan to the world PMS 1Y/ IDE 5Y VIABAHN 治験市販後調査から:JETTALKs ONAIR 2020.
- Ohki T, Kichikawa K, Yokoi H, et al. Outcomes of the Japanese multicenter Viabahn trial of endovascular stent grafting for superficial femoral artery lesions. Journal of Vascular Surgery 2017;66(1):130-142.e1.
本資料に示される情報は完全なものではなく、すべての症例に適用できるものではありません。また、電子添文および各症例に関する医療関係者の専門的な判断の代替となるものでもありません。各患者への医療行為に関するすべての判断は、それを行う各医療関係者の責任に属するものであり、当社はこれらに関する判断、助言等を行うものではありません。
本ウェブサイトは医療関係者向けです。全ての禁忌、警告、使用上の注意および有害事象に関する詳細は電子化された添付文書(電子添文)を必ずご参照ください。電子添文は常に最新版であることを、こちらからご確認ください。
弊社製品のご使用にあたっては、一部を除いて、関連学会によって策定された適正使用指針に定められた資格要件を満たしていただく必要があり、さらに弊社が提供する教育プログラムの終了が必須となります。
販売名:ゴア® バイアバーン® ステントグラフト
承認番号:22800BZX00070000
一般的名称:ヘパリン使用中心循環系ステントグラフト