チャレンジングポイント
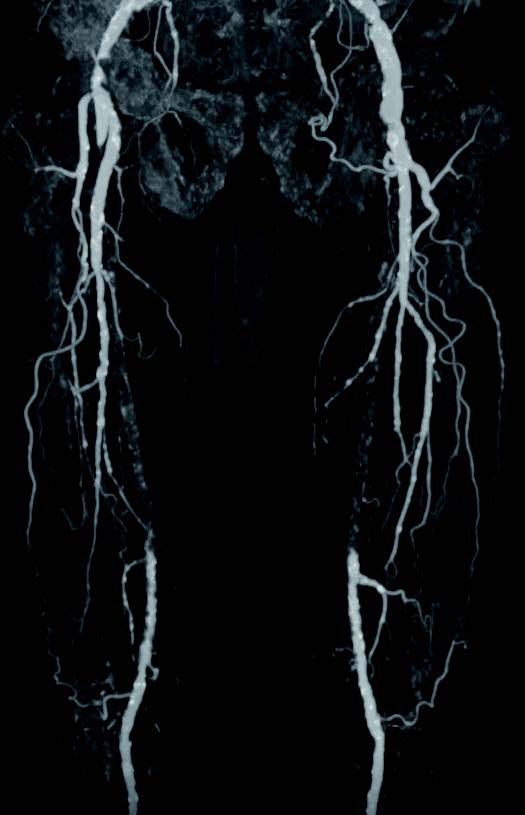
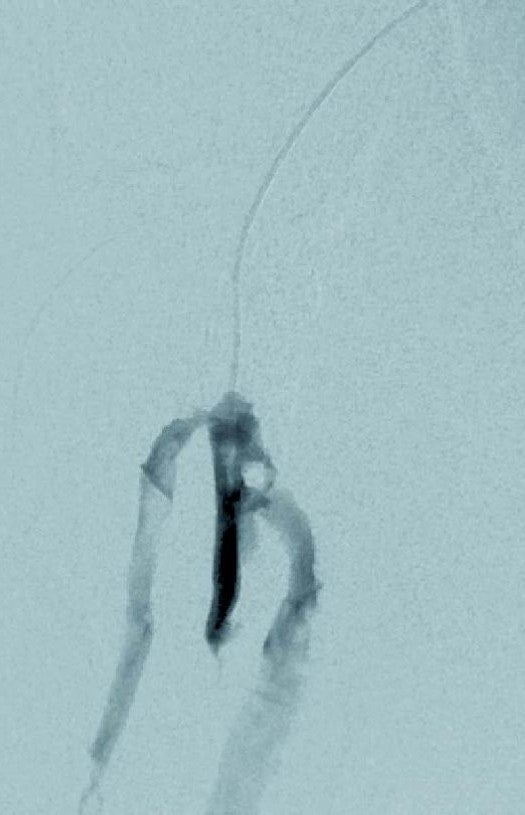
今回提示した症例のポイントは、高度石灰化病変へのバイアバーン® ステントグラフトの留置である。高度石灰化病変は、薬剤コーティングバルーン(DCB)においても、薬剤溶出型ステント(DES)においても、自施設での経験から良好な成績が得られていないと考える。高度石灰化病変に対する治療成績は、さまざまな病変の複雑性による治療成績の差を縮めることが期待できるバイアバーン® ステントグラフトの最も特徴的な部分を表している。(図1、 図2)

患者背景・病変背景
- 年齢 : 80歳代 性別 : 男性
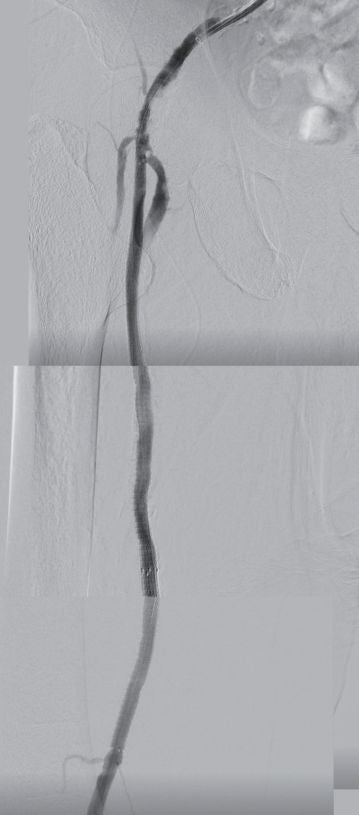
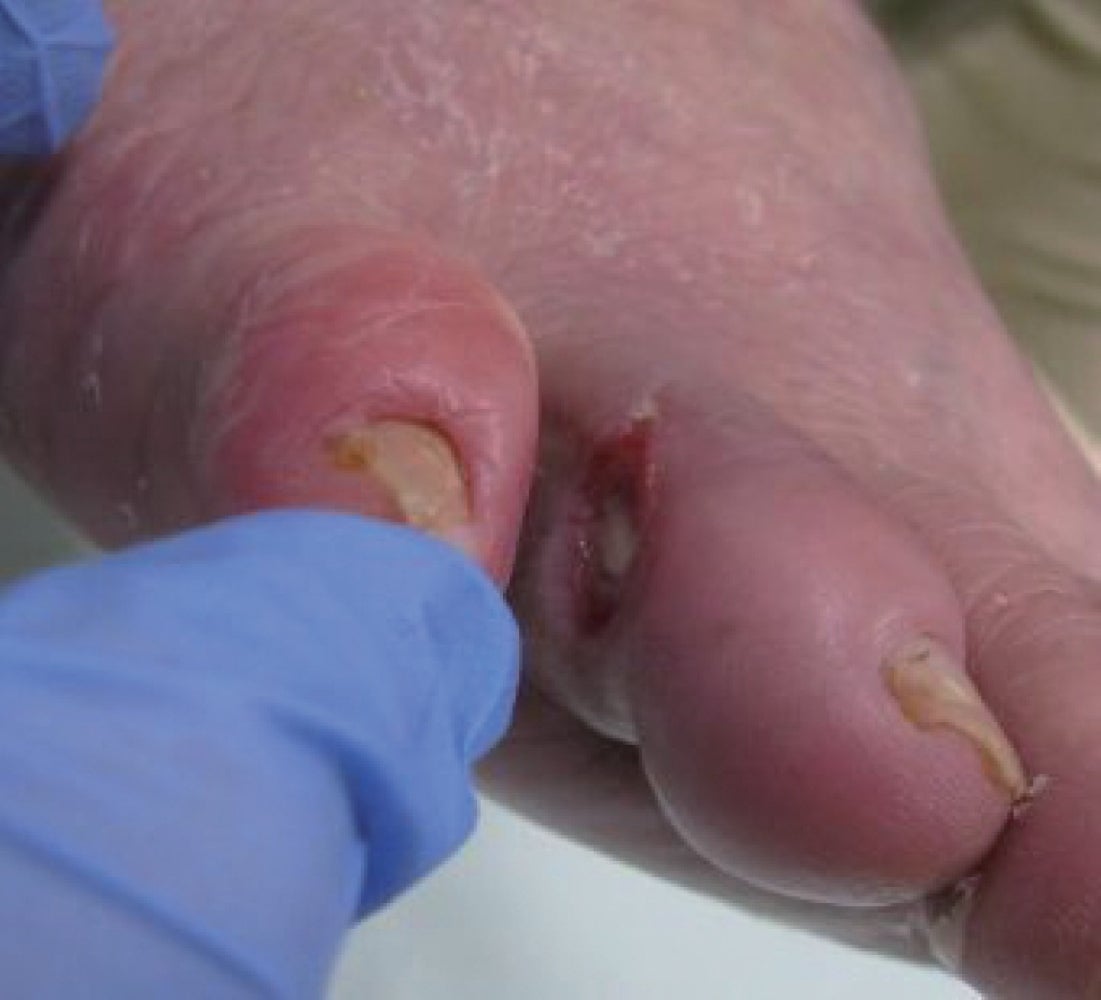
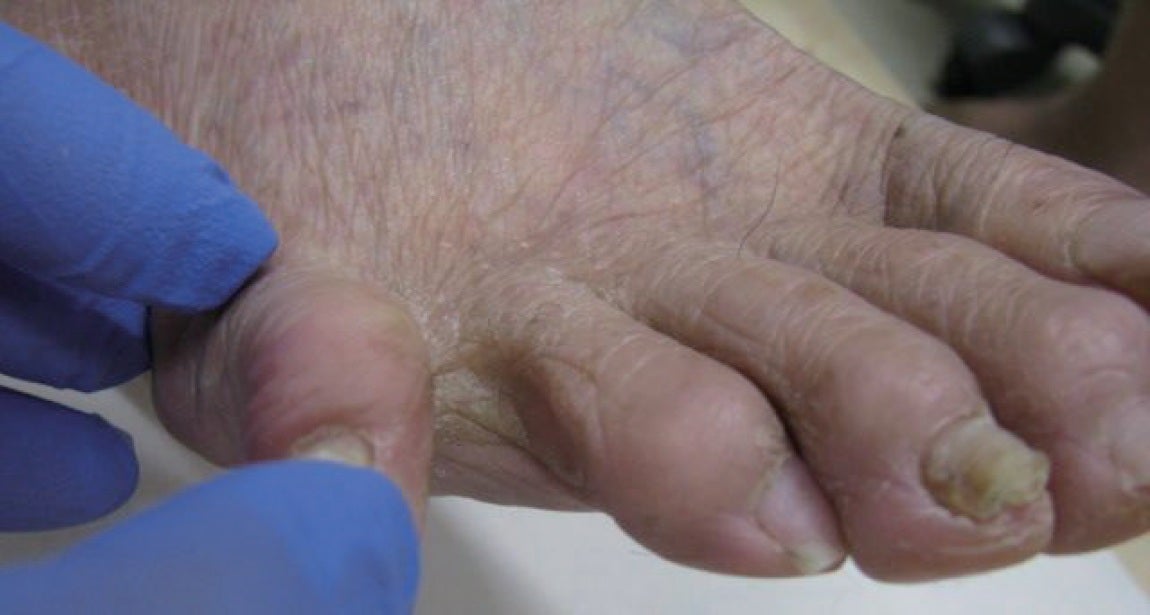
- 右第4足趾の潰瘍で紹介。包括的高度慢性下肢虚血(CLTI)と診断(図3)
- Rutherford 分類 : 5
- 対象病変部位 : 右浅大腿動脈(SFA)の慢性完全閉塞病変(CTO) TASC Ⅱ D
- 病変長 : 292 mm。SFA 入口部は10 mm ほどあり、中枢130 mm 程度までの石灰化は軽度であったが、それ以降は SFA 末梢まで高度石灰化を呈していた。
- リスク因子 : 慢性腎疾患、大腸がん術後
- ABI 測定値 : 0.66
- SPP 測定値 : 足底23 mmHg/ 足背29 mmHg
治療内容
右CFAの狭窄が疑われたため、対側の左CFA逆行性アプローチとした。6 Frガイティングカテーテル45 cmを山越えし、右EIAに留置した。右CFAの造影で石灰化による有意狭窄を認めたため、6 mm × 20 mmのcutting balloonで十分に拡張した。続いて、右SFAは10 mmほどの入口部を認めたため、慎重にCTO proximal capにアプローチした。同部位より5.5 Frインナーガイディングカテーテル、0.014 inchガイドワイヤー対応のIVUS、0.014 inchのCTO用ワイヤーの組み合わせで、入口部のtrue lumenを確保しCTOに侵入した。IVUS knuckle法でtrue lumenであることを確認しながらガイドワイヤーを進めた。
入口部からアテローム性血栓内を130 mmほど進んだところで高度石灰化部位に到達した。同部位は4 Fr造影カテーテル、0.035 inchのガイドワイヤー(先端Jカーブ)の組み合わせで石灰化を滑らせるように抜けた。最後のdistal capは0.014 inchのCTO 用ワイヤーでdrillingしてtrue lumenへ抜けた。
病変長が290 mmと長く、石灰化が高度であったこと、中枢のhealthy landingが10 mm長かったことからバイアバーン® ステントグラフトを選択した。3 mm × 300 mmのバルーンで前拡張するもバイアバーン® ステントグラフトは通過しなかったため、5 mm × 300 mmバルーンで拡張し、さらに0.018 inchのスティッフタイプのガイドワイヤーに入れ替えバイアバーン® ステントグラフトをdeliveryした。末梢にバイアバーン® ステントグラフト5 mm × 150 mmおよび、中枢側に6 mm × 250 mmを留置し病変をフルカバーした。5 mm × 300 mmのバルーンで20気圧まで圧を上げてしっかり後拡張を行った。
IVUSでminimum stent area(MSA)に13.3 mm2と一部の拡張不全を認めたが、血流が良好であったため問題ないと判断した。BKはATA、PTAが閉塞し、PAのみ開存していた。CLTIであったことからBKへの治療介入も検討したが、PAからの側副血行路が良好であったことから介入しなかった。手術時間は147分であった。
バイアバーン® ステントグラフトの選択理由
DCBおよびDESでの治療では、自施設での経験からは長期の開存を期待するのが難しいと思われる高度石灰化の病変であった。バイアバーン® ステントグラフトは、過去の報告から高度石灰化病変が開存率損失の要因として認められておらず1、また、入口部がしっかりと残存していたことから適応と考えた。また、CLTIであり創部の治癒のために最低でも半年から1年のpatencyを確保せねばならず、その点からもバイアバーン® ステントグラフトを選択すべきであると考えた。
使用デバイス
- ガイディングシース : 6 Fr 45 cm
- インナーガイディングカテーテル : 5.5 Fr(入口部)
- 造影カテーテル 4 Fr(高度石灰病変部)
- 前拡張バルーン : 径3.0/ 長300 mm → 径5.0/ 長300 mm
- ステント : バイアバーン® ステントグラフト :
- 径5.0/ 長150 mm(末梢側)
- 径6.0/ 長250 mm(中枢側)
- 後拡張バルーン : 径5.0/ 長300 mm
- その他 : 0.014 inch ガイドワイヤー用 IVUS
フォローアップ詳細
術後よりアスピリン/クロピドグレルのDAPTを開始した。ABIは0.96まで改善した。創部の経過観察を行い改善傾向であることを確認して術後5日目に退院となった。外来で創部の観察を行い、術後1か月で潰瘍は乾燥し、3か月後には上皮化し治癒した(図4)。ABIは良好に維持され、0.92(3か月後)、0.87(12か月後)、0.91(18か月後)であった。術後6か月および12か月後のデュプレックス法による超音波検査でも再狭窄は認めず、良好な血流が維持されていた。
考察
当院において2017年5月~2019年11月にバイアバーン® ステントグラフトを留置したSFA症例は42例であり、12か月のprimary patencyは80.0%、CD-TLR freeは82.9%であった。複雑病変も含まれており、実臨床上の成績としては良好と考えられた。
再狭窄のリスク因子を検討したところ、石灰化の指標であるPACSS gradeでの治療成績の差は認めなかった。また、MSAにおいても成績の差を認めず、今回の症例のように高度石灰化病変に留置したバイアバーン® ステントグラフトでは内腔が狭小化することがあるが、有意な再狭窄因子とはならないことが示唆された。唯一、他のデバイスとの併用が再狭窄因子としてあげられた点は、過去の報告1と一致した(自施設データ / 非閉塞群:7.3%、閉塞群:42.6%;P =0.044)。
今回提示した症例のポイントは、高度石灰化病変へのバイアバーン® ステントグラフトの留置である。本稿の執筆時点では、高度石灰化病変に対する治療に関してはDCBにおいても、DESにおいても自施設の経験からは良好な成績が得られていないと考える。また、過去の報告を含めたこれまでの研究において、バイアバーン® ステントグラフトは高度石灰化が再狭窄のリスク因子となっていない。このことは我々の研究において、バイアバーン® ステントグラフトの内腔狭小化がリスク因子となっていないことに一致すると考える。なぜなら、高度石灰化病変にバイアバーン® ステントグラフトを留置した際には内腔狭小化を伴うことが多いからである。
高度石灰化病変に対する治療成績は、さまざまな病変の複雑性による治療成績の差を縮めることが期待できるバイアバーン® ステントグラフトの最も特徴的な部分を表していると考える。
- lida O, Takahara M, Soga Y, et al; VANQUISH Investigators. One-year outcomes of heparin-bonded stent-graft therapy for real-world femoropopliteal lesions and the association of patency with the prothrombotic state based on the prospective, observational, multicenter Viabahn Stent-Graft Placement for Femoropopliteal Diseases Requiring Endovascular Therapy (VANQUISH) Study. Journal of Endovascular Therapy 2021;28(1):123-131.
本資料に示される情報は完全なものではなく、すべての症例に適用できるものではありません。また、電子添文および各症例に関する医療関係者の専門的な判断の代替となるものでもありません。各患者への医療行為に関するすべての判断は、それを行う各医療関係者の責任に属するものであり、当社はこれらに関する判断、助言等を行うものではありません。
本ウェブサイトは医療関係者向けです。全ての禁忌、警告、使用上の注意および有害事象に関する詳細は電子化された添付文書(電子添文)を必ずご参照ください。電子添文は常に最新版であることを、こちらからご確認ください。
弊社製品のご使用にあたっては、一部を除いて、関連学会によって策定された適正使用指針に定められた資格要件を満たしていただく必要があり、さらに弊社が提供する教育プログラムの終了が必須となります。
販売名:ゴア® バイアバーン® ステントグラフト
承認番号:22800BZX00070000
一般的名称:ヘパリン使用中心循環系ステントグラフト