治療戦略と長期予後観察の一例
SFAの長区域閉塞病変にゴア® バイアバーン® ステントグラフトを留置し、3年フォローした一例
チャレンジングポイント
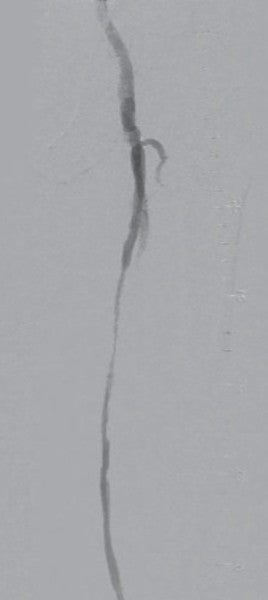
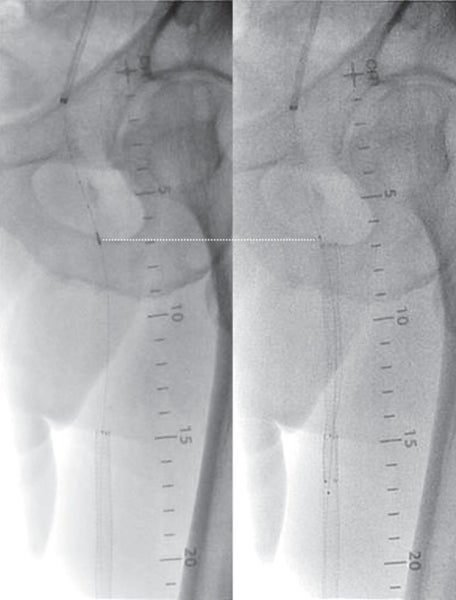
比較的若年のSFA-CTO症例であったが、患者は低侵襲であるEVTを希望された。 仕事が多忙とのことであり、何度もEVTを行うのは難しい状況のため、できるだけバイアバーン® ステントグラフト留置によって長期開存が得られるよう十分な内腔の確保、healthy landingを念頭に、将来的に万一閉塞した場合に備えて側副血行路の温存を考えた。(図1、2)

患者背景・病変背景
- 年齢 : 69歳
- 性別 : 男性
- 対象病変部位 : 左 EIA: 90%、 左 SFA ostium 〜 distal CTO
- リスク因子 : 糖尿病
- Rutherford 分類 : 3度 重度間歇性跛行
- TASC Ⅱ分類 : C
- 病変長 : 22 cm
- その他症状 : 慢性心房細動
治療戦略
術前のCTAでは左EIAに高度狭窄を認めたため、対側CFAアプローチとした。腸骨動脈領域はびまん性高度石灰化を伴っていたが、大腿膝窩領域にはSFA遠位部にスポットな石灰化を認めるのみであった。CTOに対するワイヤリングに際して、当院では使用するデバイスの種類にかかわらず十分なデバイス拡張を得るためにIVUSガイドワイヤリングを行い、intraplaqueを通過するよう心がけている。ただし、本症例は心房細動の既往もあり血栓性病変である可能性も考えられたため、ガイドワイヤー通過後にIVUSでプラークの診断を行い、必要があれば末梢保護デバイスの使用を考慮することとした。
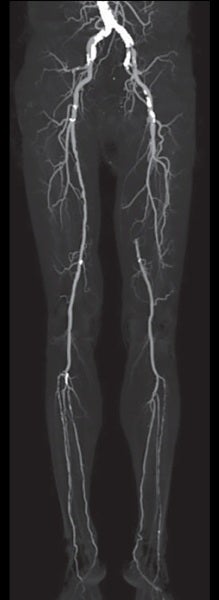
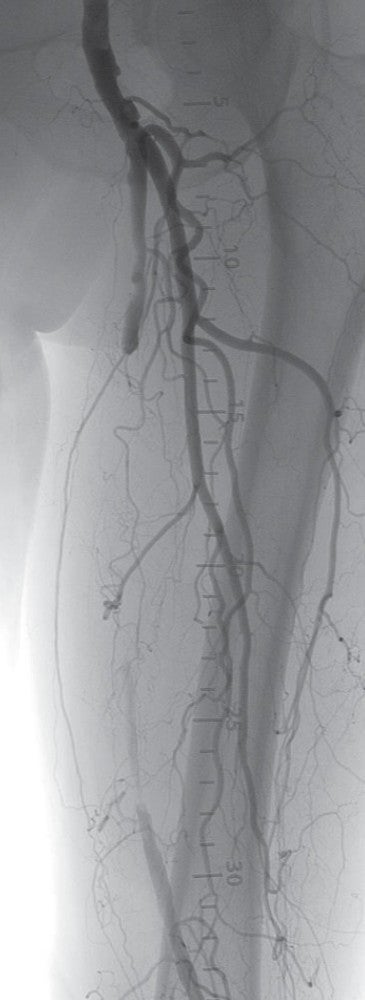
実際の治療:
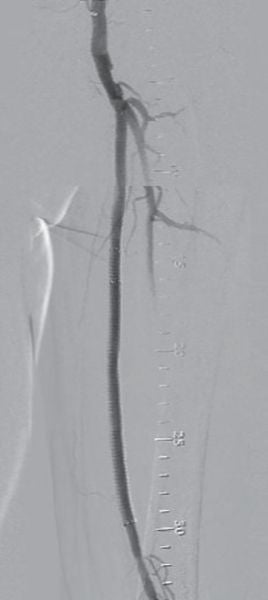
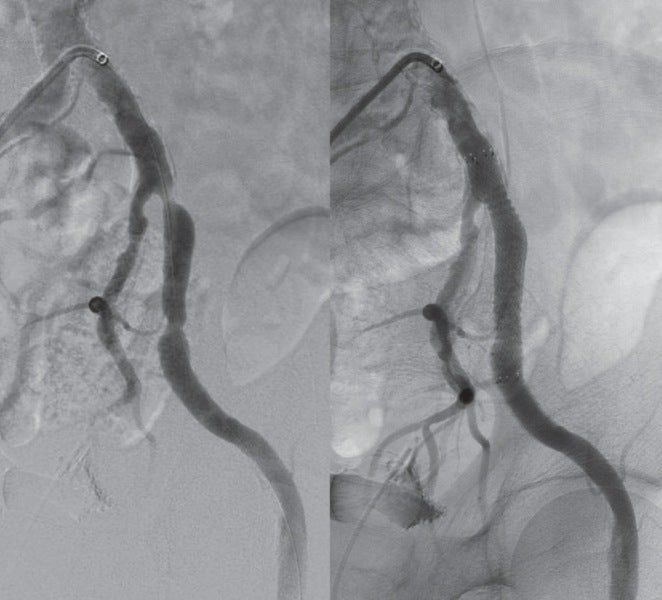
対側CFAより6 Fr 45 cm長のガイディングシースを挿入し山越えにて左EIA遠位部に進めた。この時点で圧波形は問題なかったため、手技を継続することとした。まず、5.5 Fr 100 cm長のガイディングカテーテルのバックアップ下、IVUSガイドに0.014 inchガイドワイヤー(先端荷重3 gポリマージャケットタイプ)を進めたところ、比較的容易にガイドワイヤー通過に成功した。IVUSでは全長にわたり intraplaqueを通過していたものの、血栓成分の多いプラークと考えられた。このため、5.5 FrのガイディングカテーテルをSFA遠位部に先進し、フィルターワイヤー(径 8 mm)を膝窩動脈に留置し遠位部保護を行った。続いて、5.5 Frガイディングカテーテルを用いて血栓吸引を行ったうえで、小径バルーン径 4.0 mm / 長 220 mmを使用し6 atmで前拡張した。(図3)この時点で造影にて末梢塞栓のないことを確認しフィルターワイヤーを回収、0.035 inchガイドワイヤーを用いて7 Fr 55 cm長のガイディングシースへ交換した。0.014 inchガイドワイヤー(先端荷重 1 g 親水性コートタイプ)を挿入後、SFA遠位よりバイアバーン® ステントグラフト径 7.0 mm / 長 150 mmを留置し、バルーン径 6.0 mm / 長 80 mmを用いてステントグラフト内のみ 18 atmで後拡張を行った。続いて、SFA近位部のlanding zoneをIVUSマーキングしたうえで、(図4)バイアバーン® ステントグラフト径 7.0 mm / 長 100 mmを追加留置した。先述のバルーン径 6.0 mm / 長 80 mmを用いて高圧拡張の後、近位部のみバルーン径 7.0 mm / 長 100 mmを使用し12 atmで後拡張を追加した。IVUSにてステントグラフトの拡張が良好かつmalpositionがないことを確認した。 最後に、EIAに対してベアメタルステント(BMS)径 10 mm / 長 60 mmを留置、後拡張を行って手技を終了した。(図5、6)
バイアバーン® ステントグラフト選択理由
CTAではSFA起始部、遠位部ともにhealthy landingが可能と予想された。また、TASC分類C病変であり、良好な長期開存率を参考1、2にバイアバーン® ステントグラフトを使用する方針とした。Landing zoneについては、IVUSを用いhealthy intimaを同定、また可能な限り側副血行路を塞がないように留置することを心がけた。
使用デバイス
- ガイディングシース:6 Fr 45 cm → 7 Fr 55 cm
- ガイドワイヤー:
- 0.035 inch、長 300 cm(先端形状 1.5 mm Jカーブ)、
- 0.014 inch、長 230 cm(先端荷重 3 g ポリマージャケットタイプ)、
- 0.014 inch、長 300 cm(先端荷重 1 g 親水性コートタイプ)
- 前拡張バルーン:径 4.0 mm / 長 220 mm(セミコンプライアントバルーン)
- ステント:
- バイアバーン® ステントグラフト径 7.0 mm / 長 150 mm 1本
- バイアバーン® ステントグラフト径 7.0 mm / 長 100 mm 1本
- 後拡張バルーン:
- 径 6.0 mm / 長 80 mm(ノンコンプライアントバルーン)、
- 径 7.0 mm / 長 100 mm(セミコンプライアントバルーン)
- その他:
- IVUS、フィルターワイヤー 径 8 mm、止血デバイス 7 Fr シース対応等
- EIAにベアメタルステント 径 10 mm / 長 60 mm
留置後3年までの患者フォローアップ詳細
ABI 値
左術前 0.58 → 術後 1.02 → 1Y 0.95 → 2Y 0.96 → 3Y 1.07
DUS フォローアップ
PSVR 1M 0.70 / 3M 0.82 / 6M 1.70 / 12M 0.60
抗血栓薬プロトコール
~1M : アピキサバン 5 mg × 2、アスピリン 100 mg、クロピドグレル硫酸塩 75 mg
1~12M : アピキサバン 5 mg × 2、クロピドグレル硫酸塩 75 mg
12M~ : アピキサバン 5 mg × 2
コメント
比較的血栓成分の多いSFAのCTO病変であり、遠位塞栓をいかに予防するかを考える必要があった。遠位塞栓の予防方法としては、フィルターデバイスの使用あるいは外部からの物理的圧迫が挙げられるが、今回は患者負担も考慮しフィルターデバイスを使用した。また、血栓吸引後の前拡張では小径バルーンを用いて、できるだけ低圧で行い、後拡張でもバイアバーン® ステントグラフト径より1 mmアンダーサイズのバルーンを使用した。また、近位端のみ同径サイズのバルーンを使用することすることにより、血栓成分を飛ばさないように配慮した。バイアバーン® ステントグラフトは理論的にはグラフト素材によるメカニカルバリア機能によって病変を押さえ込むことができると考えられるため、他デバイスに比し血栓が多く含まれる可能性のある病変でも適しているデバイスと考えられる。ほか、バイアバーン® ステントグラフトの位置決めについては、DFAならびに側副血行路を塞がないように正確に留置することが望ましいが、当院においては必ずIVUSマーキングを行って正確なデバイスの位置決めを心がけており、本症例でも正確な位置に留置することができた。本症例は、患者の職業上、運動量が多く治療前は業務に支障をきたしていたが、術後は完全に症状が消失し業務遂行が可能になったとのことであった。現在、 外来にて3年フォローが完了しているが、良好な経過を維持できている。
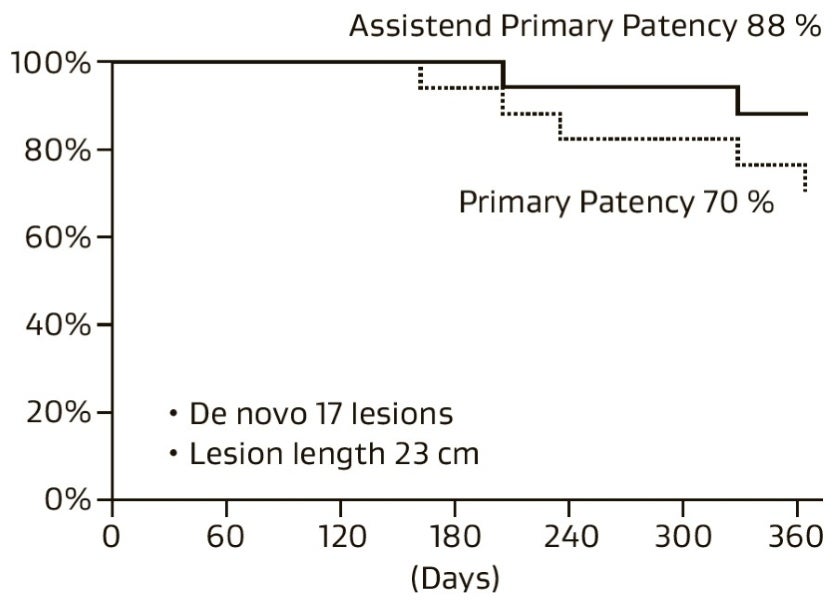
一般的にバイアバーン® ステントグラフトは、20 cmを超えるような長病変であっても、良好な開存率が報告されている数少ないデバイスであり1、2、本邦における実臨床を反映したVANQUISH studyにおいても、平均病変長25 cmの病変に対し1年時の1次開存率は 80%と良好な成績が報告されている3。ただし、本研究では病変をバイアバーン® ステントグラフトでフルカバーしたほうが開存率が良好であることが示されており、使用に際してはバイアバーン® ステントグラフトによるフルカバーが可能である適切な病変を選択することが重要と考えられる。また、術後の血栓性閉塞については 6%の症例にみられたものの、複雑な病変背景にもかかわらず大切断はわずかに 0.3%とのことであった3。当院では、バイアバーン® ステントグラフト留置例に対しては、開存維持と血栓性閉塞の予防のため、外来でDUS(Duplex Ultra Sound)による定期フォローを行っており、エッジ部狭窄(PSVR > 2.5)を認めた場合は、メンテナンスEVTを行うよう努めている。当院においても、De novo症例に対するバイアバーン® ステントグラフトの臨床成績は、1年次のAssisted Primary Patency 88%と非常に良好であった(図7)。
当院では、術後抗血栓薬については、添付文書を参考に1年間のDAPT(Dual Anti-Platelet Therapy)、以降は抗血小板薬1剤を継続している。また、抗凝固療法併用例では、3剤併用はできるだけ短期間とし、1年までは2剤併用療法を行い、以降は抗凝固薬単剤としている。
治療前後の造影動画
- Lammer, J., Zeller, T., Hausegger, K.A. et al. Sustained Benefit at 2 Years for Covered Stents Versus Bare-Metal Stents in Long SFA Lesions: The VIASTAR Trial. Cardiovasc Intervent Radiol 38, 25–32 (2015)
- Ohki T, Kichikawa K, Yokoi H, et al. Outcomes of the Japanese multicenter Viabahn trial of endovascular stent grafting for superficial femoral artery lesions. Journal of Vascular Surgery 2017;66(1):130-142.e1.
- Iida O, Takahara M, Soga Y, et al; VANQUISH Investigators. One-year outcomes of heparin-bonded stent-graft therapy for real-world femoropopliteal lesions and the association of patency with the prothrombotic state based on the prospective, observational, multicenter Viabahn Stent-Graft Placement for Femoropopliteal Diseases Requiring Endovascular Therapy (VANQUISH) Study. Journal of Endovascular Therapy 2021, Vol. 28(1) 123–131
本資料に示される情報は完全なものではなく、すべての症例に適用できるものではありません。また、電子添文および各症例に関する医療関係者の専門的な判断の代替となるものでもありません。各患者への医療行為に関するすべての判断は、それを行う各医療関係者の責任に属するものであり、当社はこれらに関する判断、助言等を行うものではありません。
本ウェブサイトは医療関係者向けです。全ての禁忌、警告、使用上の注意および有害事象に関する詳細は電子化された添付文書(電子添文)を必ずご参照ください。電子添文は常に最新版であることを、こちらからご確認ください。
弊社製品のご使用にあたっては、一部を除いて、関連学会によって策定された適正使用指針に定められた資格要件を満たしていただく必要があり、さらに弊社が提供する教育プログラムの終了が必須となります。
販売名:ゴア® バイアバーン® ステントグラフト
承認番号:22800BZX00070000
一般的名称:ヘパリン使用中心循環系ステントグラフト