治療戦略と長期予後観察の一例
浅大腿動脈入口部近位からの長区域慢性完全閉塞病変に対するゴア® バイアバーン® ステントグラフト留置の一例
チャレンジングポイント
浅大腿動脈入口部近位からの閉塞病変であり、側副血行路の深大腿動脈の血流を維持すること。腎機能障害(ステージ4)を合併しており、最小限の造影剤で治療を完遂すること。

患者背景・病変背景
- 年齢:70 歳代 性別:女性
- 動脈硬化リスク因子:慢性腎臓病(ステージ4、eGFR22)、高血圧症
- 併発疾患:原発性胆汁性肝硬変
- EVT歴:前年、左右腸骨動脈自己拡張型ステント留置
- 対象病変:左浅大腿動脈入口部近位からの長区域慢性完全閉塞病変
- Rutherford 4 TASC II D
治療戦略
右大腿動脈穿刺からの山越えアプローチを選択。体表面エコーで確実に浅大腿動脈入口部真腔を同定し、ガイドワイヤーを進める。最小限の造影剤使用とするため、閉塞病変部にガイドワイヤーを進め、血管内超音波で真腔を通過していることを確認。バルーンで前拡張を行った後、ゴア® バイアバーン® ステントグラフトを病変部位をフルカバーするように留置した。
使用デバイス
- ガイディングカテーテル:6 Fr 60 cm(山越えアプローチで使用)
- ガイドワイヤー:0.035 inch(ガイディングカテーテル誘導用)、0.014 inch 長 300 cm、エクステンションワイヤー(血管狭窄部貫通用カテーテル併用)
- 貫通デバイス:血管狭窄部貫通用カテーテル、マイクロカテーテル
- 前拡張バルーン:径 2.0/長 20 mm、径 4.0/長 250 mm(セミコンプライアント)、径 3.0 /長 40 mm(ノンコンプライアント)
- ステントグラフト:径 5.0 mm /長 250 mm バイアバーン® ステントグラフト
- 後拡張バルーン:長 250 mm(セミコンプライアント)
- 血管内超音波
治療内容
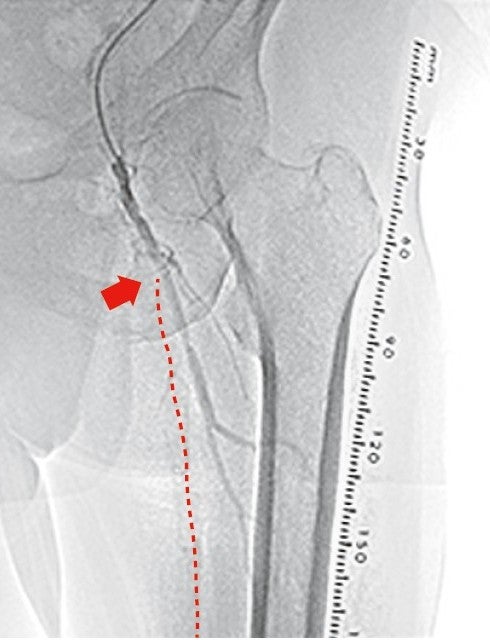
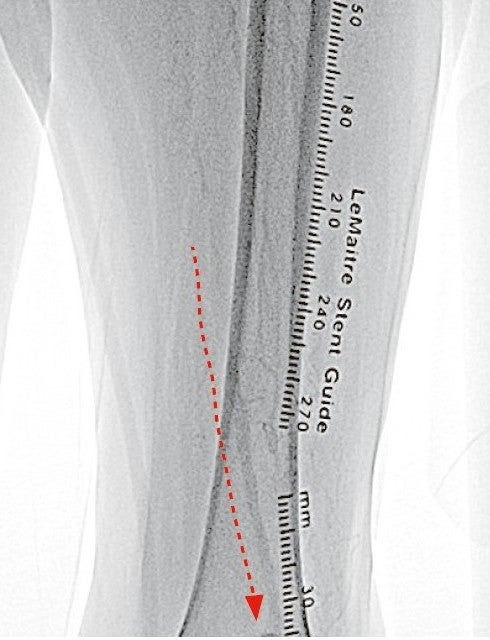
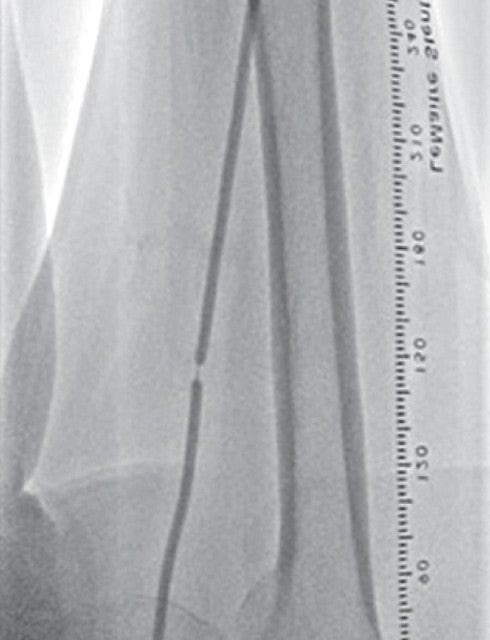
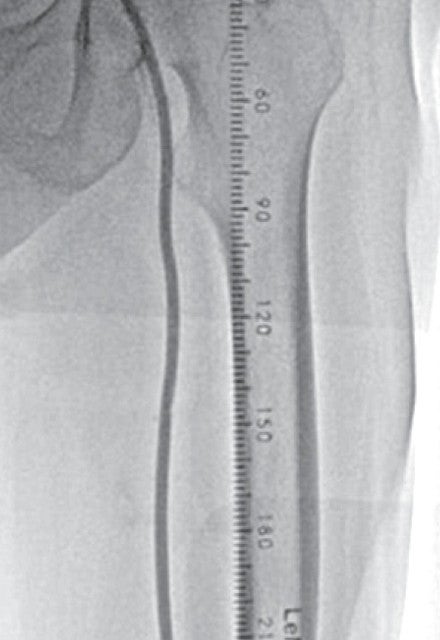
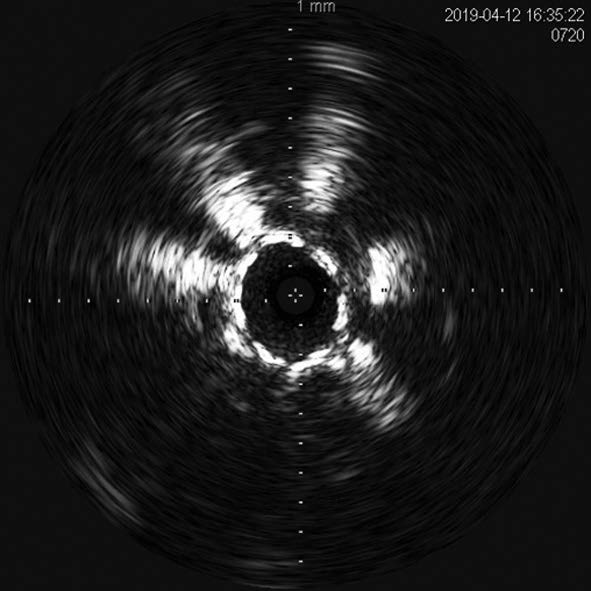
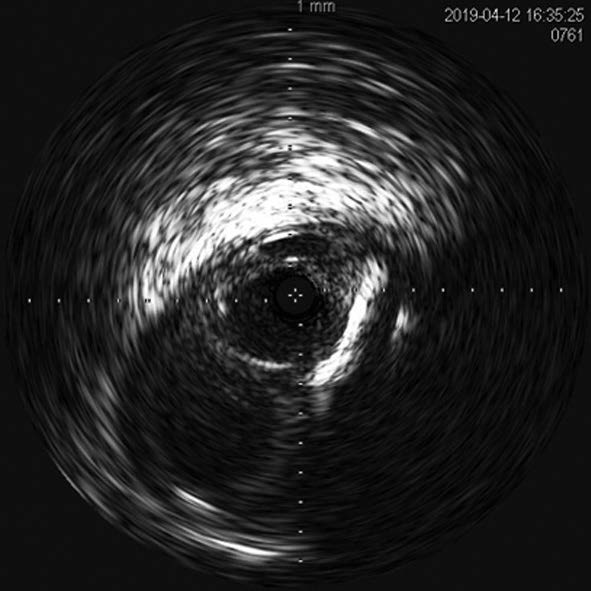
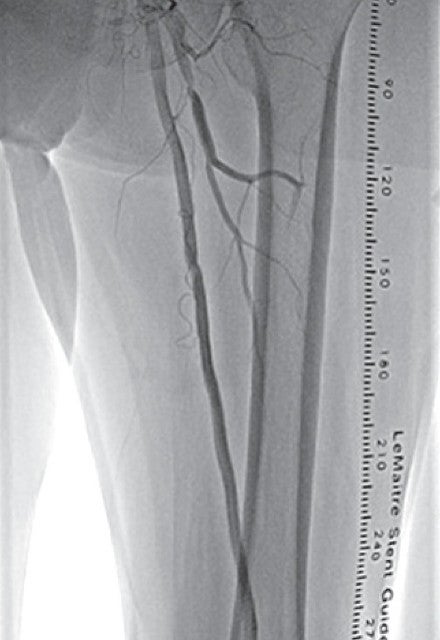
右大腿動脈穿刺、0.035 inchワイヤーを用いて、ガイディングシース 6 Fr 60 cmを左外腸骨動脈まで誘導し、造影を行った(図1.2)。体表面エコーガイドのもと、マイクロカテーテルと0.014 inch フロッピー300 cmワイヤーで、確実に浅大腿動脈入口部から血管真腔内を進めた。0.014 inch フロッピー300 cmワイヤーを抜去し、血管狭窄部貫通用カテーテルに交換し、閉塞部位を慎重に進め、貫通に成功した。血管狭窄部貫通用カテーテルにエクステンションワイヤーをつなげ、マイクロカテーテルを抜去、0.018 inchの径 2.0/長 20 mmバルーンで閉塞部位を拡張した。マイクロカテーテルを末梢まで進め、血管狭窄部貫通用カテーテルを抜去、0.014 inch 300 cm ワイヤーに交換、血管内超音波で病変部の観察を行った。ほぼ真腔を捉えていることが確認できたため、径 4.0/長 250 mmバルーンで閉塞全域を拡張した。一部石灰化病変により、拡張不良部位を認めたため(図3)、径 3.0/長 40 mm ノンコンプライアントバルーンで追加拡張を行った。再度、径 4.0/長 250 mmバルーンで閉塞全域を拡張した(図4)。血管内超音波で閉塞領域を観察し、ほぼ真腔を捉えていることが確認できた。ついで、径 5.0/長 250 mmバイアバーン® ステントグラフトを留置し、グラフト内をバルーンで後拡張した。血管内超音波でグラフト拡張および浅大腿動脈入口部を確認した(図5.6)。結果、左浅大腿動脈の良好な血流を得た(図7)。
手技時間:144 分 造影剤使用量:40 ml 透視時間:37 分
留置後1年半までの患者フォローアップ詳細
体表面エコーでのフォローアップ : 1か月後、3か月後、6か月後、9か月後、1年後、1.5年後にチェックし、すべて開存確認し得た。
血圧脈波(ABI):治療前 0.78、1か月後 0.98、1.5年後 0.92と大きな変化なく、安定している。
抗血小板剤 : 6か月間はクロピドグレルとサルポグレラートの2剤併用、6か月後よりクロピドグレル 75 mg単剤としている。
コメント
浅大腿動脈の長区域慢性完全閉塞病変に対するバイアバーン® ステントグラフトは、最長で250 mmの製品サイズがあり、有用なデバイスであると考える。浅大腿動脈入口部近位から閉塞している例が多いので、体表面エコーを使って、確実にワイヤーを真腔に導き、閉塞部位を貫通できたら、十分な前拡張を行った上で、バイアバーン® ステントグラフトを留置することが重要である。また、バイアバーン® ステントグラフトは狙った位置への留置が容易なことが特徴の一つであると考える。
治療前後の造影動画
本資料に示される情報は完全なものではなく、すべての症例に適用できるものではありません。また、電子添文および各症例に関する医療関係者の専門的な判断の代替となるものでもありません。各患者への医療行為に関するすべての判断は、それを行う各医療関係者の責任に属するものであり、当社はこれらに関する判断、助言等を行うものではありません。
本ウェブサイトは医療関係者向けです。全ての禁忌、警告、使用上の注意および有害事象に関する詳細は電子化された添付文書(電子添文)を必ずご参照ください。電子添文は常に最新版であることを、こちらからご確認ください。
弊社製品のご使用にあたっては、一部を除いて、関連学会によって策定された適正使用指針に定められた資格要件を満たしていただく必要があり、さらに弊社が提供する教育プログラムの終了が必須となります。
販売名:ゴア® バイアバーン® ステントグラフト
承認番号:22800BZX00070000
一般的名称:ヘパリン使用中心循環系ステントグラフト