Klinische Daten zur GORE® PROPATEN® Gefäßprothese: Daten zu infragenualen Bypässen
GORE® PROPATEN® Gefäßprothese: Primäre Offenheitsrate bei infragenualen Bypässen
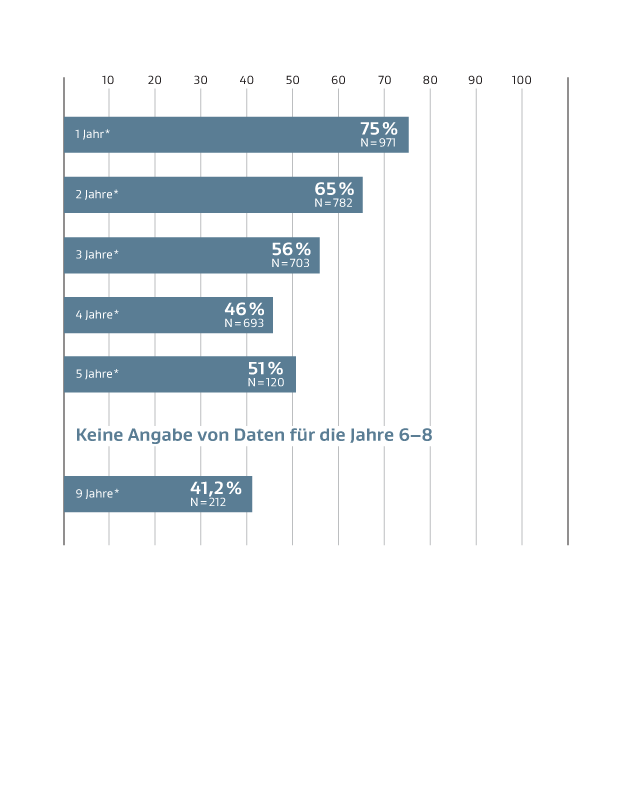
* Der gewichtete Gesamtmittelwert der primären Offenheitsraten basiert auf Daten aus 10 Fachveröffentlichungen (peer-reviewed), bei denen vorab definierte Einschlusskriterien erfüllt waren.
Die Studiengröße (N) entspricht der anfänglichen Kohortengröße der Studie.
Daten zu infragenualen Bypässen | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Studie | Jahr | Ort | N | Primäre Offenheitsrate | |||||
| Jahr 1 | Jahr 2 | Jahr 3 | Jahr 4 | Jahr 5 | Jahr 9 | ||||
| Kaisar et al | 2018 | Infrapopliteal | 62 | 85 % | 71 % | 64 % | 57 % | ||
| Uhl et al | 2015 | Infrapopliteal | 89 | 64 % | 49 % | 34 % | |||
| Neville et al | 2014 | Infrapopliteal | 62 | 75 % | |||||
| Monaca et al | 2013 | Infrapopliteal | 212 | 52 % | 41 % | ||||
| Dorigo et al | 2012 | Infragenual fem-pop Infrapopliteal | 414 142 | 45 % 39 % | |||||
| Pulli et al | 2010 | Infragenual fem-pop Infrapopliteal | 238 86 | 75 % 66 % | 67 % 57 % | 61 % 52 % | |||
| Daenens et al | 2009 | Infragenual fem-pop Infrapopliteal | 57 97 | 92 % 79 % | 83 % 69 % | ||||
| Hugl et al | 2009 | Infragenual fem-pop Infrapopliteal | 37 15 | 74 % 79 % | |||||
| Lösel-Sadée et al | 2009 | Infragenual fem-pop Infrapopliteal | 30 45 | 77 % 64 % | 71 % 57 % | 71 % 50 % | 71 % 50 % | 71 % 50 % | |
| Peeters et al | 2008 | Infragenual fem-pop Infrapopliteal | 41 37 | 86 % 71 % | 79 % 60 % | 75 % 60 % | |||
Einschlusskriterien
Einschlusskriterien für die in dieser Analyse verwendeten Daten zu infragenualen, femoropoplitealen (fem-pop) und infrapoplitealen GORE® PROPATEN® Gefäßprothesen:
- Artikel mit Peer-Review in medizinischen Zeitschriften in englischer Sprache
- Sich nicht überschneidende Patientenpopulationen
- Die primäre Offenheitsrate des infragenualen Bypasses wurde für mindestens 12 Follow-up-Monate erfasst.
- N = 50 oder mehr infragenuale Bypässe (infragenual-femoropopliteal und infragenual-femorodistal) im Behandlungsarm mit der GORE® PROPATEN® Gefäßprothese

Eine vollständige Beschreibung aller geltenden Indikationen, Warnhinweise, Vorsichtsmaßnahmen und Kontraindikationen für die Länder, in denen dieses Produkt angeboten wird, finden Sie in der Gebrauchsanweisung unter eifu.goremedical.com. RXOnly
INDIKATIONEN IN EUROPA: Die GORE® PROPATEN® Gefäßprothese ist für Patienten vorgesehen, die aufgrund von Gefäßverschlüssen oder Aneurysmen oder nach Traumata einen Ersatz bzw. Bypass für periphere Gefäße benötigen, oder für Patienten, die nach terminalem Nierenversagen einen arteriovenösen Hämodialysezugang in den oberen oder unteren Extremitäten benötigen.
Die GORE® PROPATEN® Gefäßprothese zur Verwendung als pädiatrischer Shunt ist für die stufenweise palliative Behandlung von angeborenen zyanotischen Herzfehlern (CCHD) vorgesehen.
KONTRAINDIKATIONEN: Die GORE® PROPATEN® Gefäßprothese darf bei Patienten mit bekannter Überempfindlichkeit gegen Heparin NICHT verwendet werden und auch nicht bei Patienten, bei denen eine heparininduzierte Thrombozytopenie (HIT) vom Typ II aktuell vorliegt oder aus der Anamnese bekannt ist.
Alle folgenden Ausführungen der GORE® PROPATEN® Gefäßprothese dürfen NICHT als Bypässe für Koronararterien oder bei Rekonstruktionseingriffen an den Hirngefäßen eingesetzt werden:
- GORE® PROPATEN® Gefäßprothese mit integrierten Ringen
- GORE® PROPATEN® Gefäßprothese mit festen Ringen
- GORE® PROPATEN® Gefäßprothese mit abnehmbaren Ringen
- Axillobifemorale GORE® PROPATEN® Gefäßprothese mit abnehmbaren Ringen
Die GORE® PROPATEN® Gefäßprothese darf NICHT als Patch verwendet werden. Wird die GORE® PROPATEN® Gefäßprothese zerschnitten und als Patch verwendet, verfügt sie möglicherweise nicht über eine ausreichende Scherfestigkeit.
FÜR PATCH-ANWENDUNGEN: Für kardiovaskuläre Eingriffe, bei denen Verschlussmaterial erforderlich ist, steht der GORE® ACUSEAL kardiovaskuläre Patch zur Verfügung.