Occlusioni totali croniche dell'SFA
Consideri la complessità di trattare le occlusioni totali croniche (CTO)
- Le CTO possono aumentare la necessità di stenting provvisorio.1
- Nello studio Medtronic IN.PACT Global Study, il trattamento delle CTO ha aumentato dell'85% il tasso di stenting provvisori.
- Sebbene sia una complicanza rara, è stato dimostrato che il rischio di embolizzazione distale aumenta durante il trattamento di una CTO.2-3
- I dati di confronto tra le tecnologie endovascolari più recenti e il bypass chirurgico – il trattamento attualmente raccomandato per le CTO – sono limitati.4
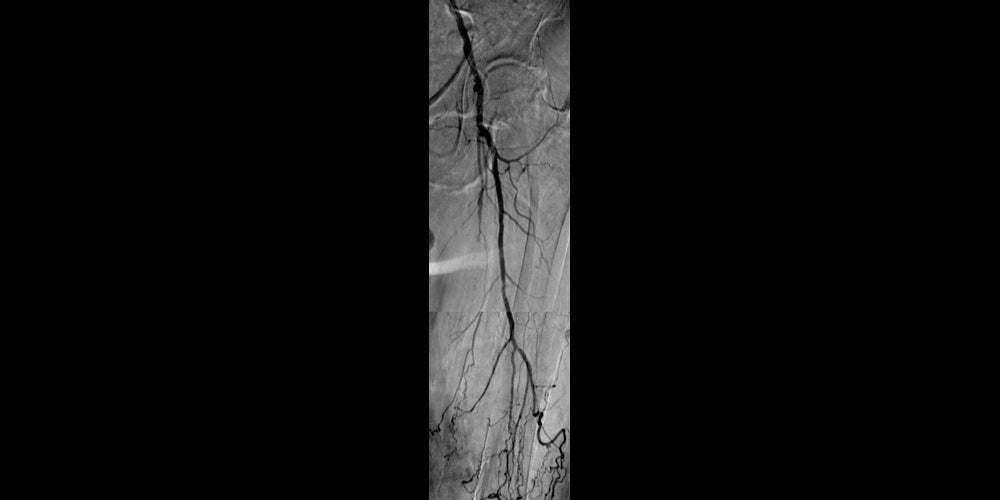
Prima
CTO dell'SFA sinistra con deflusso di un solo vaso (non mostrato).
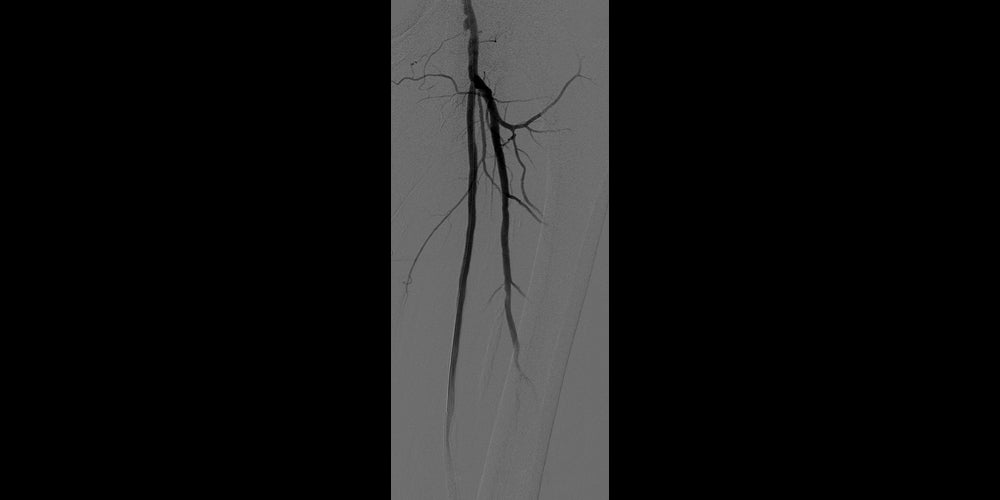
Dopo
Dopo il posizionamento di due endoprotesi GORE® VIABAHN® con superficie PROPATEN* di 6 mm x 15 cm. Mantenuto il deflusso di un solo vaso. (non mostrato)
La protesi VIABAHN® è stata ampiamente studiata nelle CTO5-9
Pervietà comprovata
il 72% degli arti studiati in 5 studi multicentrici, prospettici, randomizzati o a braccio singolo presentavano CTO (302/422) che hanno raggiunto il
75% di pervietà primaria5-9
Durabilità dimostrata
97%
Pervietà secondaria a 3 anni nella patologia complessa
(27 cm lunghezza media delle lesioni, 93% di CTO).10
Risultati clinici sovrapponibili al bypass chirurgico sopragenicolare (vena protesica11 e nativa5).
Il design della protesi VIABAHN® è unicamente in grado di trattare le CTO
- Il lume ematico in PTFE espanso (ePTFE) copre e sigilla la trombosi residua.
- La superficie eparinata CBAS®, che caratterizza anche la protesi vascolare GORE® PROPATEN®, è la comprovata e duratura tecnologia per legare l'eparina, concepita appositamente per resistere alla formazione di trombi.12
* Come inteso da GORE, superficie bioattiva PROPATEN si riferisce alla superficie eparinata CBAS® di proprietà di Gore.
- Brodmann M. Real world value of the In.Pact Admiral DCB (Medtronic) for fem-pop lesions: from the In.Pact Global Registry: what else does it tell us. Presentato al 44th Annual Symposium on Vascular and Endovascular Issues, Techniques, Horizons (VEITH symposium); November 14-18, 2017; New York, NY.
- Wu W, Hua S, Li Y, et al. Incidence, risk factors, treatment and prognosis of popliteal artery embolization in the superficial femoral artery interventions. PLoS One 2014;9(9):e107717.
- Shrikhande GV, Khan SZ, Hussain HG, Dayal R, McKinsey JF, Morrissey N. Lesion types and device characteristics that predict distal embolization during percutaneous lower extremity interventions. Journal of Vascular Surgery 2011;53(2):347-352.
- Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG; TASC II Working Group. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). Journal of Vascular Surgery 2007;45(1)Supplement:S5-S67.
- Reijnen M, van Walraven L, Fritschy W, et al. 1-year results of a multicenter, randomized controlled trial comparing heparin-bonded endoluminal to femoropopliteal bypass. Journal of Cardiovascular Interventions 2017;10(22):2320-2331.
- Ohki T, Kichikawa K, Yokoi H, et al. Outcomes of the Japanese multicenter Viabahn trial of endovascular stent grafting for superficial femoral artery lesions. Journal of Vascular Surgery 2017;66(1):130-142.e1.
- Saxon RR, Chervu A, Jones PA, et al. Heparin-bonded, expanded polytetrafluoroethylene-lined stent graft in the treatment of femoropopliteal artery disease: 1year results of the VIPER (Viabahn Endoprosthesis with Heparin Bioactive Surface in the Treatment of Superficial Femoral Artery Obstructive Disease) Trial. Journal of Vascular & Interventional Radiology 2013;24(2):165-173.
- Lammer J, Zeller T, Hausegger KA, et al. Sustained benefit at 2 years for covered stents versus bare-metal stents in long SFA lesions: the VIASTAR trial. Cardiovascular & Interventional Radiology 2015;38(1):25-32.
- Zeller T, Peeters P, Bosiers M, et al. Heparin-bonded stent-graft for the treatment of TASC II C and D femoropopliteal lesions: the Viabahn25 cm Trial. Journal of Endovascular Therapy 2014;21(6):765774.
- Istruzioni per l'uso (IFU) dell'endoprotesi GORE® VIABAHN® con superficie eparinica bioattiva. W. L. Gore & Associates, Inc. Data di accesso: 8 febbraio 2023. https://eifu.goremedical.com
- McQuade K, Gable D, Pearl G, Theune B, Black S. Four-year randomized prospective comparison of percutaneous ePTFE/nitinol self-expanding stent graft versus prosthetic femoral-popliteal bypass in the treatment of superficial femoral artery occlusive disease. Journal of Vascular Surgery 2010;52(3):584-591.
- Superficie eparinata CBAS®. Riferimenti. W. L. Gore & Associates, Inc. Data di accesso: 24 marzo 2023. https://www.goremedical.com/cbas/references

Per una descrizione completa di tutte le indicazioni, le avvertenze, le precauzioni e le controindicazioni vigenti nei mercati in cui il prodotto è disponibile, consultare le Istruzioni per l'uso sul sito eifu.goremedical.com. RXOnly
INDICAZIONI PER L'USO IN EUROPA: L'endoprotesi GORE® VIABAHN® con superficie bioattiva PROPATEN è indicata per il trattamento di:
- lesioni de novo o ristenotiche delle arterie iliache
- lesioni de novo o ristenotiche dell'arteria femorale superficiale e dell'arteria poplitea prossimale
- lesioni ristenotiche intrastent dell'arteria femorale superficiale e dell'arteria poplitea prossimale
- stenosi o occlusione trombotica nell'anastomosi venosa della protesi sintetica per l'accesso arterovenoso (AV) e nel deflusso venoso dei circuiti di accesso per dialisi, comprese le vene centrali
- aneurismi dell'arteria poplitea e aneurismi isolati delle arterie viscerali
- lesioni vasali traumatiche o iatrogene delle arterie che sono posizionate nella cavità toracica, addominale o pelvica (con l'eccezione di aorta, coronarie, tronco arterioso brachiocefalico, carotidi, arterie vertebrali e polmonari)
CONTROINDICAZIONI:
- Nelle lesioni non complianti, laddove un pallone per angioplastica non abbia raggiunto l'espansione completa durante la predilatazione, oppure qualora fosse impossibile dilatare le lesioni in misura sufficiente per consentire il passaggio del sistema di rilascio.
- L'endoprotesi GORE® VIABAHN® con superficie bioattiva PROPATEN non deve essere utilizzata in pazienti con nota ipersensibilità all'eparina, compresi i pazienti che hanno manifestato un precedente evento di trombocitopenia indotta da eparina (HIT) di tipo II.