Denken Sie daran, wie kompliziert es ist, chronische Totalverschlüsse (CTO) zu behandeln.
- CTO können die Notwendigkeit einer provisorischen Stentimplantation erhöhen.1
- In der globalen IN.PACT-Studie von Medtronic erhöhte die Behandlung von CTO die Rate einer provisorischen Stentimplantation um 85 %.
- Obwohl es sich um eine seltene Komplikation handelt, hat sich erwiesen, dass das Risiko einer distalen Embolisation bei der Behandlung von CTO erhöht ist.2-3
- Es gibt nur begrenzte Vergleichsdaten zwischen neueren endovaskulären Technologien und operativen Bypässen, der aktuell empfohlenen Behandlung bei CTO.4
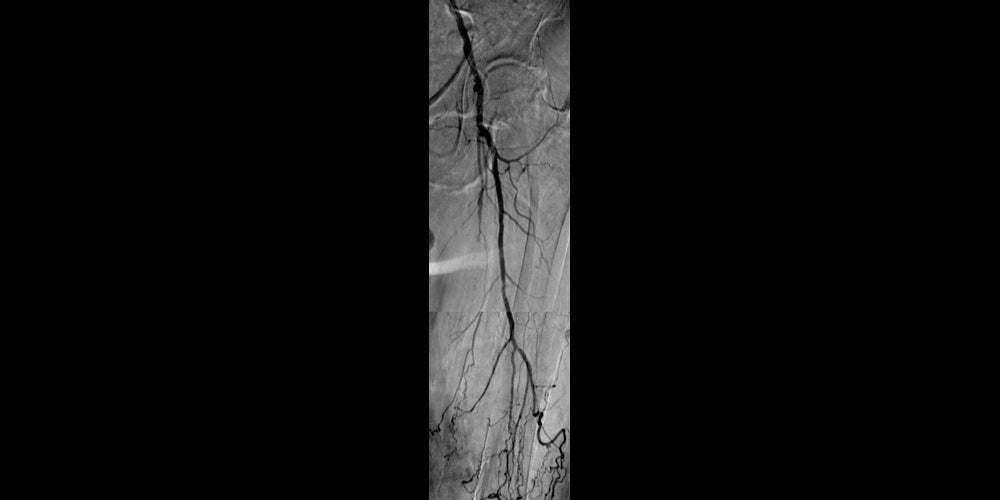
Vorher
Linker AFS-CTO mit Ein-Gefäßabstrom (nicht abgebildet).
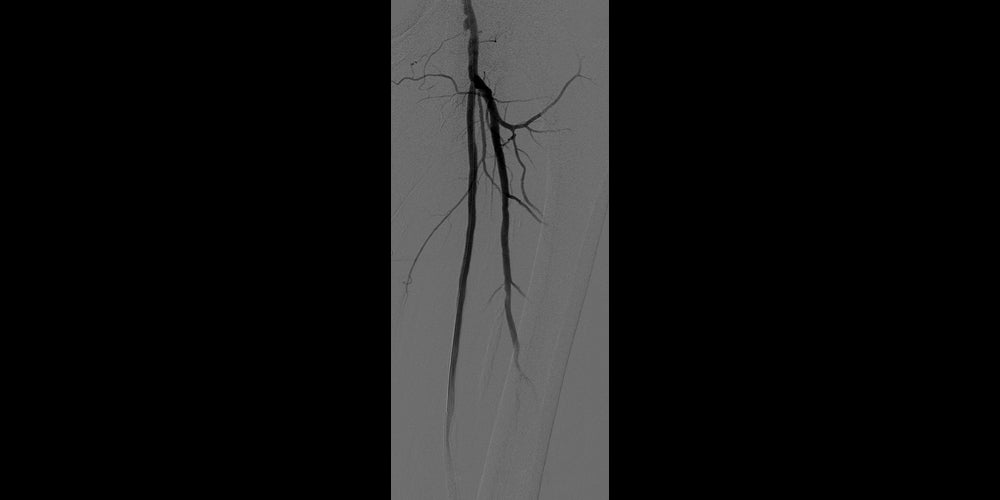
Nachher
Nach der Platzierung von zwei 6 mm x 15 cm GORE® VIABAHN® Endoprothesen mit bioaktiver PROPATEN Oberfläche*. Ein-Gefäßabstrom erhalten (nicht abgebildet).
Das VIABAHN® Implantat wurde bei CTO ausgiebig untersucht.5-9
Nachweisliche Offenheit
72 % untersuchte Extremitäten aus 5 multizentrischen, prospektiven, randomisierten oder einarmigen Studien – CTO (302/422) – erreichten.
75 % primäre Offenheit5-9
Nachgewiesene Langlebigkeit
97 %
Sekundäre Offenheit bei komplizierten Erkrankungen nach 3 Jahren.
(27 cm durchschnittliche Läsionslänge, 93 % CTO).10
Vergleichbare klinische Ergebnisse mit supragenualem operativem Bypass (sowohl prothetische11 als auch native Venen5).
Das Design des VIABAHN® Implantats ist auf einzigartige Weise für die Behandlung von CTO geeignet
- Das Blutflusslumen aus expandiertem PTFE (ePTFE) deckt Restthrombose ab und verschließt diese.
- Die CBAS®‑Heparin‑Oberfläche, die auch die GORE® PROPATEN® Gefäßprothese aufweist, ist die bewährte nachhaltige Heparinbindungstechnologie, die darauf ausgelegt ist, die Bildung von Thromben zu verhindern.12
* Bioaktive PROPATEN Oberfläche bezieht sich bei Gore auf die firmeneigene CBAS®‑Heparin‑Oberfläche.
- Brodmann M. Real world value of the In.Pact Admiral DCB (Medtronic) for fem-pop lesions: from the In.Pact Global Registry: what else does it tell us. Präsentiert beim 44. Annual Symposium on Vascular and Endovascular Issues, Techniques, Horizons (VEITH symposium); 14.–18. November 2017; New York, NY.
- Wu W, Hua S, Li Y, et al. Incidence, risk factors, treatment and prognosis of popliteal artery embolization in the superficial femoral artery interventions. PLoS One 2014;9(9):e107717.
- Shrikhande GV, Khan SZ, Hussain HG, Dayal R, McKinsey JF, Morrissey N. Lesion types and device characteristics that predict distal embolization during percutaneous lower extremity interventions. Journal of Vascular Surgery 2011;53(2):347-352.
- Norgren L, Hiatt WR, Dormandy JA, Nehler MR, Harris KA, Fowkes FG; TASC II Working Group. Inter-Society Consensus for the Management of Peripheral Arterial Disease (TASC II). Journal of Vascular Surgery 2007;45(1)Supplement:S5-S67.
- Reijnen M, van Walraven L, Fritschy W, et al. 1-year results of a multicenter, randomized controlled trial comparing heparin-bonded endoluminal to femoropopliteal bypass. Journal of Cardiovascular Interventions 2017;10(22):2320-2331.
- Ohki T, Kichikawa K, Yokoi H, et al. Outcomes of the Japanese multicenter Viabahn trial of endovascular stent grafting for superficial femoral artery lesions. Journal of Vascular Surgery 2017;66(1):130-142.e1.
- Saxon RR, Chervu A, Jones PA, et al. Heparin-bonded, expanded polytetrafluoroethylene-lined stent graft in the treatment of femoropopliteal artery disease: 1year results of the VIPER (Viabahn Endoprosthesis with Heparin Bioactive Surface in the Treatment of Superficial Femoral Artery Obstructive Disease) Trial. Journal of Vascular & Interventional Radiology 2013;24(2):165-173.
- Lammer J, Zeller T, Hausegger KA, et al. Sustained benefit at 2 years for covered stents versus bare-metal stents in long SFA lesions: the VIASTAR trial. Cardiovascular & Interventional Radiology 2015;38(1):25-32.
- Zeller T, Peeters P, Bosiers M, et al. Heparin-bonded stent-graft for the treatment of TASC II C and D femoropopliteal lesions: the Viabahn25 cm Trial. Journal of Endovascular Therapy 2014;21(6):765774.
- GORE® VIABAHN® Endoprothese mit bioaktiver Heparin-Oberfläche Gebrauchsanweisung. W. L. Gore & Associates, Inc. Letzter Zugriff am 8. Februar 2023. https://eifu.goremedical.com
- McQuade K, Gable D, Pearl G, Theune B, Black S. Four-year randomized prospective comparison of percutaneous ePTFE/nitinol self-expanding stent graft versus prosthetic femoral-popliteal bypass in the treatment of superficial femoral artery occlusive disease. Journal of Vascular Surgery 2010;52(3):584-591.
- CBAS®-Heparin-Oberfläche. Referenzen. W. L. Gore & Associates, Inc. Letzter Zugriff am 24. März 2023. https://www.goremedical.com/cbas/references

Eine vollständige Beschreibung aller geltenden Indikationen, Warnhinweise, Vorsichtsmaßnahmen und Kontraindikationen für die Länder, in denen dieses Produkt angeboten wird, finden Sie in der Gebrauchsanweisung unter eifu.goremedical.com. RXOnly
INDIKATIONEN IN EUROPA: Die GORE® VIABAHN® Endoprothese mit bioaktiver PROPATEN Oberfläche ist zur Behandlung in den folgenden Fällen indiziert:
- De-novo-Läsionen oder restenotische Läsionen der Iliakalarterien
- De-novo-Läsionen oder restenotische Läsionen der A. femoralis superficialis und der proximalen A. poplitea
- Restenotische In-Stent-Läsionen der A. femoralis superficialis und der proximalen A. poplitea
- Stenose oder thrombotischer Verschluss an der venösen Anastomose synthetischer arteriovenöser Gefäßprothesen (AV-Zugänge) und im venösen Abstrom bei Shunts von Dialysezugängen, einschließlich der zentralen Venen
- Poplitealarterienaneurysmen und isolierte Viszeralarterienaneurysmen
- Traumatische oder iatrogene Gefäßschädigungen von Arterien, die sich in der Brusthöhle, im Bauchraum oder im Becken befinden (außer Aorta, Koronararterien, Truncus brachiocephalicus, Karotiden, A. vertebralis und A. pulmonalis)
KONTRAINDIKATIONEN:
- Nicht-elastische Läsionen, bei denen während der Prädilatation keine vollständige Aufdehnung des Angioplastie-Ballonkatheters erzielt wurde bzw. bei denen die Läsion nicht ausreichend aufgedehnt werden kann, um die Passage des Applikationssystems zu ermöglichen.
- Die GORE® VIABAHN® Endoprothese mit bioaktiver PROPATEN Oberfläche darf bei Patienten mit bekannter Überempfindlichkeit gegen Heparin nicht verwendet werden. Dies gilt insbesondere auch für die Patienten, bei denen in der Vergangenheit eine heparininduzierte Thrombozytopenie (HIT) vom Typ II aufgetreten ist.