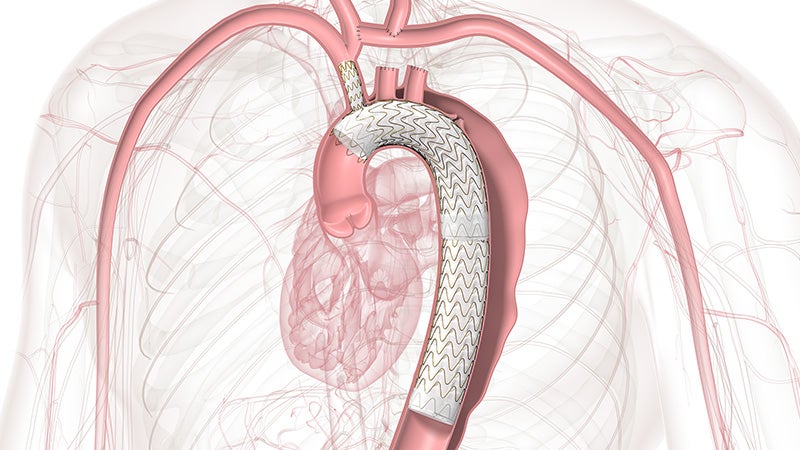
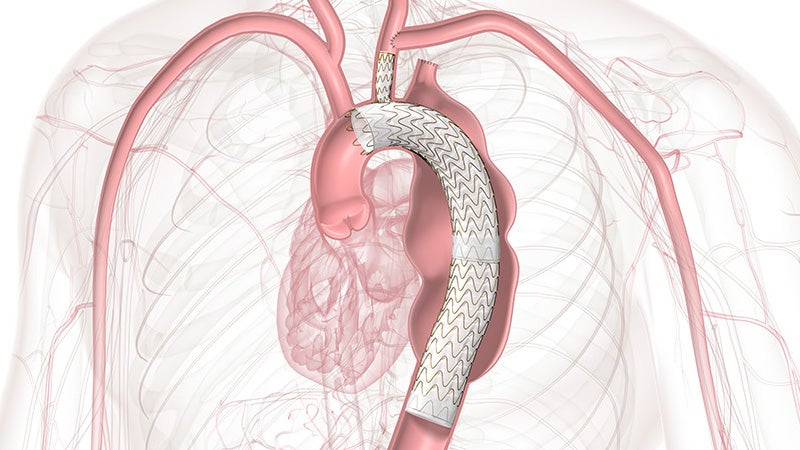
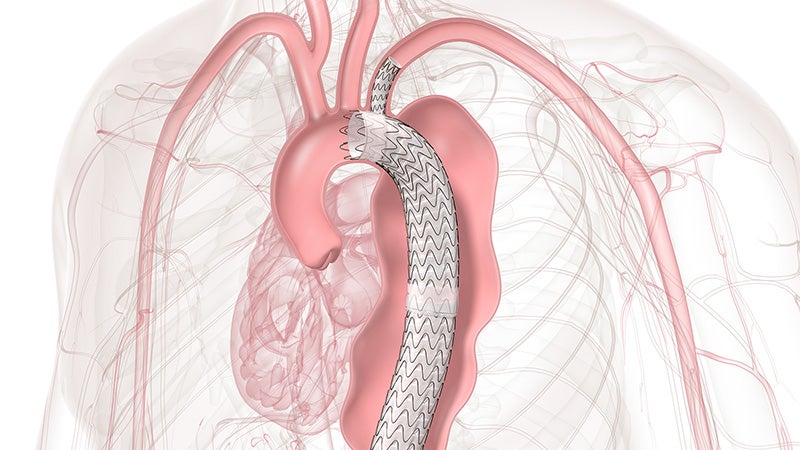
GORE® TAG® Thorakale Branch-Endoprothese
Eine einfache Lösung zum Greifen nah

Zugelassen für alle Zonen des Aortenbogens
Die bei Ärzten bewährte serienmäßige Endoprothese mit einem einzelnen Seitenast für gebranchte TEVAR-Verfahren der Zone 2 ist nun auch für die Zonen 0 und 1 zugelassen, was die minimalinvasive Reparatur für alle Läsionen des Aortenbogens ermöglicht.
Die TBE bietet Ärzten eine zulassungskonforme endovaskuläre Option zur Perfusion eines einzelnen Zielgefäßes mit geringerer Belastung der Zonen 0 und 1 durch Verringerung der Gesamtbelastung bei Eingriffen wie Sternotomie, kardiopulmonalem Bypass und Kreislaufstillstand.
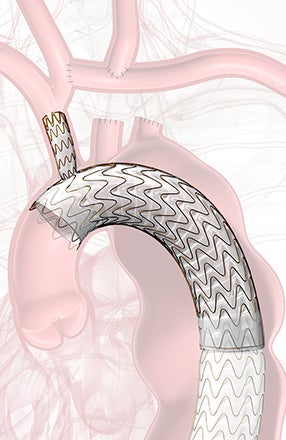
Die TBE bietet eine anerkannte Lösung zur Aufrechterhaltung des Blutflusses zur LSA ohne das potenzielle Risiko und die Komplexität der operativen Revaskularisierung.

Die erste Endoprothese dieser Art – zugelassen gemäß FDA und der europäischen Medizinprodukte-Verordnung mit CE-KENNZEICHNUNG, konzipiert für vereinfachte, minimalinvasive TEVAR-Eingriffe in Zone 2. Erzielen Sie optimale Ergebnisse ohne das potenzielle Risiko und die Komplexität der Revaskularisierung.
Serienmäßige endovaskuläre Prothesen sind herkömmlichen chirurgischen Optionen zum Erhalt der LSA vorzuziehen.
durchschnittliche Verringerung der Länge von Krankenhausaufenthalten4
potenzielle Verringerung der OP-Zeit4
Wie die Technologie der Einzelverzweigung das Leben eines Patienten in einer Notfallsituation beeinflusste.
Der schrittweise offene und TEVAR-Ansatz mit der TBE bietet eine „vollständige und umfassende thorakale Lösung“ bei zahlreichen Erkrankungen.
Ob es um Zone 0, 1 oder 2 geht, ziehen Sie die TBE für Ihre nächste Reparatur des Aortenbogens in Betracht.
Von der Fallplanung bis zur implantatspezifischen Beratung stehen wir Ihnen zur Seite und unterstützen Sie.
- Schulungsbedarf – Unerlässliche technische Unterstützung mit fundierten Produktkenntnissen.
- Mehr als 8 Jahre – durchschnittliche Beschäftigungsdauer eines Außendienstmitarbeiters für Aortenprodukte von Gore, basierend auf vielfältigen klinischen Hintergründen.
- Keine Provisionen für Vertriebsmitarbeiter – wir konzentrieren uns auf Ergebnisse.

Auf dieses Produkt bezogen:
a Es war keine Intervention erforderlich.
b Vom Core Lab berichtet, 3 Jahre (Gesamt über 36 Monate (1–1275 Tage)).
c Die Reinterventionen waren Embolisation und Platzierung eines thorakalen Stent Graft.
- Butterfield K, Hsu M, Powis S, Thon M. Evaluation of the GORE® TAG® Thoracic Branch Endoprosthesis (TBE Device) in the Treatment of Lesions of the Aortic Arch (Pivotal): Zone 0/1. Flagstaff, AZ: W. L. Gore & Associates, Inc; 2024. [Studienbericht vor der Marktzulassung]. MD200865. Rev 1.
- Daten liegen vor, 2024; W. L. Gore & Associates, Inc; Flagstaff, AZ.
- Brown J, Gorman J, Sondreaal M, Powis S. Evaluation of the GORE® TAG® Thoracic Branch Endoprosthesis (TBE Device) in the Treatment of Lesions of the Descending Thoracic Aorta (Pivotal): Zone 2. Flagstaff, AZ: W. L. Gore & Associates, Inc; 2021. [SSB 11-02 Studienbericht vor der Marktzulassung]. MD185099. Rev 1.
- Squiers JJ, DiMaio JM, Schaffer JM, et al. Surgical debranching versus branched endografting in zone 2 thoracic endovascular aortic repair. Journal of Vascular Surgery 2022;75(6):1829-1836.e3.

Eine vollständige Beschreibung aller geltenden Indikationen, Warnhinweise, Vorsichtsmaßnahmen und Kontraindikationen für die Länder, in denen dieses Produkt angeboten wird, finden Sie in der Gebrauchsanweisung unter eifu.goremedical.com. RXOnly
INDIKATIONEN IN EUROPA: Die GORE® TAG® Thorakale Branch-Endoprothese ist für die endovaskuläre Behandlung aller Läsionen der thorakalen Aorta descendens indiziert (einschließlich isolierter Läsionen wie Aneurysmen und traumatische Transsektionen sowie Typ-B-Dissektionen), während bei Patienten mit geeigneter Anatomie der Blutfluss in die LSA aufrechterhalten wird.
KONTRAINDIKATIONEN: Die GORE® TAG® Thorakale Branch-Endoprothese ist in den folgenden Fällen kontraindiziert: Patienten mit bekannter Überempfindlichkeit oder Allergie gegen die Produktmaterialien [ePTFE (Polytetrafluorethylen), FEP (Fluorethylenpropylen), Nitinol (Nickel, Titan), Gold, nur SB-Komponente – Heparin (CBAS®-Heparin-Oberfläche)]; Patienten mit Erkrankungen, bei denen ein Risiko für eine Infektion der Prothese besteht; Patienten mit bekannter Überempfindlichkeit gegen Heparin einschließlich Patienten, bei denen anamnestisch eine heparininduzierte Thrombozytopenie (HIT) vom Typ II bekannt ist.