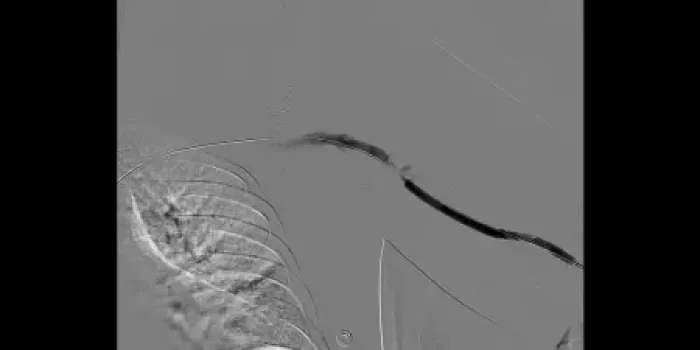
Wiederherstellung eines dauerhaften Blutflusses in der AV-Prothese nach Diagnose von Recoil nach PTA
Eine Fallstudie mit der GORE® VIABAHN® Endoprothese mit bioaktiver PROPATEN Oberfläche*
Herausforderung
Ein 70-jähriger Mann mit einer Anamnese von Diabetes mellitus, Nierenzellkarzinom und Nierenerkrankung im Endstadium stellte sich mit anhaltenden Blutungen und erhöhtem Venendruck seiner arteriovenösen Prothese (AV-Prothese) der rechten A. brachialis bis zur V. axillaris vor. Die 6-mm-AV-Prothese aus Polytetrafluorethylen (PTFE) des Patienten wurde 8 Monate vor der Vorstellung angelegt und es gab keine früheren Interventionen. Bei der ärztlichen Untersuchung war die Prothese pulsierend. Eine Doppler-Ultraschalluntersuchung ergab ein Flussvolumen der A. brachialis von 650 ml/min bei Vorliegen einer sichtbaren venösen Anastomosenstenose.
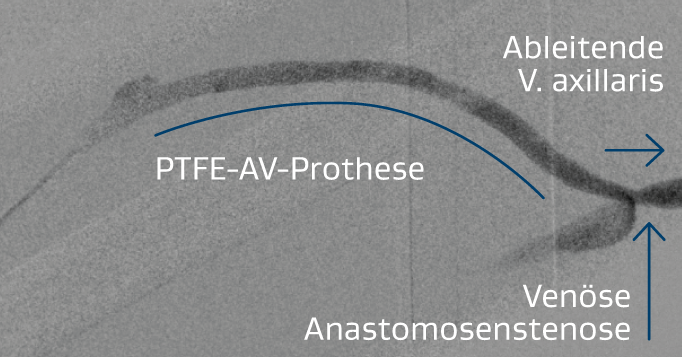
Verfahren
Angesichts der klinischen Präsentation wurde eine Angiografie durchgeführt, um eine Stenose an der venösen Anastomose zu bestätigen (Abbildung 1). Die Läsion wurde zunächst mittels perkutaner transluminaler Angioplastie (PTA) mit einem 8 x 40 mm BD® VACCESS® PTA Dilatationskatheter behandelt. Bei der Untersuchung nach der Angioplastie ist ein Recoil an der venösen Anastomose aufgefallen. Außerdem war die Prothese noch pulsierend, sodass die Entscheidung getroffen wurde, eine Endoprothese zu implantieren. Ein 8 x 50 mm VIABAHN® Implantat wurde in die venöse Anastomose vorgeschoben (Abbildung 2) und freigesetzt. Anschließend wurde eine Postdilatation mit dem 8-mm-Angioplastie-Ballon durchgeführt. Eine wiederholte Injektion eines Kontrastmittels zeigte die erfolgreiche Freisetzung der Endoprothese, wobei das Schwirren bei der körperlichen Untersuchung stärker war (Abbildung 3).

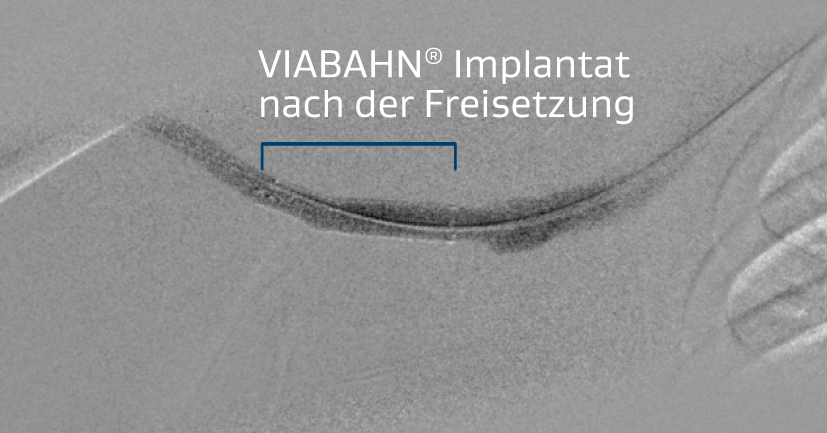
Ergebnis
Die körperliche Untersuchung bestätigte eine signifikante Verbesserung des Schwirrens durch die Prothese, wobei die Pulsatilität verringert war. Eine wiederholte Doppleruntersuchung zeigte eine Verbesserung des Blutflussvolumens der A. brachialis auf 980 ml/min. Der Patient konnte am späteren Nachmittag die Hämodialysebehandlung erfolgreich wieder aufnehmen. Sein Venendruck sank und die Blutungen an den Zugangsstellen verschwanden.
13 Monate später stellte sich der Patient aufgrund von Schwierigkeiten bei der Punktion der Prothese vor. Eine Angiografie zeigte keine signifikante Stenose innerhalb der Prothese, und der Punktionsbereich wurde für das Dialysepersonal gekennzeichnet. Es ist anzumerken, dass das in der venösen Anastomose platzierte VIABAHN® Implantat eine bleibende Offenheit zeigte, wie durch Angiografie bestätigt wurde (Abbildung 4).
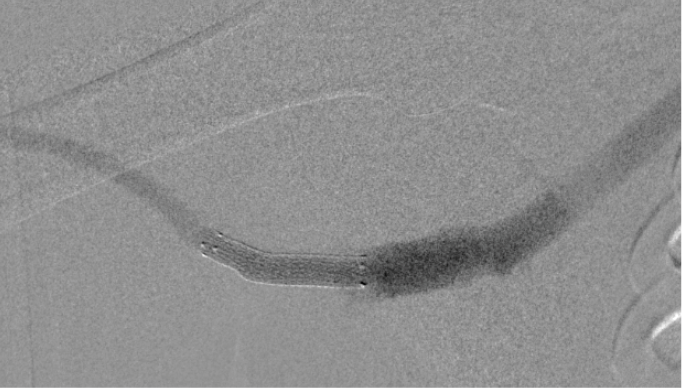
Fallpunkte
Die Behandlung der venösen Anastomose ist für die Aufrechterhaltung der Offenheit der Dialyseprothese von entscheidender Bedeutung. Eine Ballon-Angioplastie an der venösen Anastomose kann zu einem kurzfristigen Recoil, einer Restenose und einer Prothesenthrombose führen. Endoprothesen können eine nachhaltigere Behandlungsmöglichkeit darstellen. In der Gore REVISE klinischen Studie wurde nachgewiesen, dass das VIABAHN® Implantat der Ballon-Angioplastie hinsichtlich der Erhaltung der Offenheit des Zugangs überlegen war.1
Bei diesem Patienten zeigte das VIABAHN® Implantat eine Offenheit für mehr als 13 Monate, ohne dass eine Thrombose aufgetreten wäre. Das Implantat ermöglicht somit eine langlebige Behandlungsmöglichkeit für den Zugang am Ort der rezidivierenden Stenose. Für Dialysepatienten mit häufigem Versagen ihres Zugangs könnte dies einen bedeutenden Einfluss auf ihre Versorgung haben und dazu beitragen, eine längere Offenheit ihrer Prothese zu erzielen.
Relevante Fallstudien
* Bioaktive PROPATEN Oberfläche bezieht sich bei Gore auf die firmeneigene CBAS®‑Heparin‑Oberfläche.
1. W. L. Gore & Associates, Inc. GORE® VIABAHN® Endoprosthesis versus Percutaneous Transluminal Angioplasty (PTA) to Revise Arteriovenous Grafts at the Venous Anastomosis in Hemodialysis Patients. (GORE REVISE Study, AVR 06-01). Flagstaff, AZ: W. L. Gore & Associates, Inc; 2012. [Abschließender klinischer IDE-Studienbericht]. G070069.
Die Ergebnisse und Beobachtungen, über die berichtet wird, beruhen auf den Erfahrungen mit einzelnen Fällen sowie mit den behandelten Patienten. Die hier beschriebenen Schritte sind möglicherweise nicht vollständig und sind nicht als Ersatz für die Gebrauchsanweisung oder die Ausbildung, Schulung und das professionelle Urteil von Ärzten/Ärztinnen vorgesehen. Ärzte/Ärztinnen tragen allein die Verantwortung für Entscheidungen zur Behandlung der Patienten und die Verwendung medizinischer Technologien.

Eine vollständige Beschreibung aller geltenden Indikationen, Warnhinweise, Vorsichtsmaßnahmen und Kontraindikationen für die Länder, in denen dieses Produkt angeboten wird, finden Sie in der Gebrauchsanweisung unter eifu.goremedical.com. RXOnly
INDIKATIONEN IN EUROPA: Die GORE® VIABAHN® Endoprothese mit bioaktiver PROPATEN Oberfläche ist zur Behandlung in den folgenden Fällen indiziert:
- De-novo-Läsionen oder restenotische Läsionen der Iliakalarterien
- De-novo-Läsionen oder restenotische Läsionen der A. femoralis superficialis und der proximalen A. poplitea
- Restenotische In-Stent-Läsionen der A. femoralis superficialis und der proximalen A. poplitea
- Stenose oder thrombotischer Verschluss an der venösen Anastomose synthetischer arteriovenöser Gefäßprothesen (AV-Zugänge) und im venösen Abstrom bei Shunts von Dialysezugängen, einschließlich der zentralen Venen
- Poplitealarterienaneurysmen und isolierte Viszeralarterienaneurysmen
- Traumatische oder iatrogene Gefäßschädigungen von Arterien, die sich in der Brusthöhle, im Bauchraum oder im Becken befinden (außer Aorta, Koronararterien, Truncus brachiocephalicus, Karotiden, A. vertebralis und A. pulmonalis)
KONTRAINDIKATIONEN:
- Nicht-elastische Läsionen, bei denen während der Prädilatation keine vollständige Aufdehnung des Angioplastie-Ballonkatheters erzielt wurde bzw. bei denen die Läsion nicht ausreichend aufgedehnt werden kann, um die Passage des Applikationssystems zu ermöglichen.
- Die GORE® VIABAHN® Endoprothese mit bioaktiver PROPATEN Oberfläche darf bei Patienten mit bekannter Überempfindlichkeit gegen Heparin nicht verwendet werden. Dies gilt insbesondere auch für die Patienten, bei denen in der Vergangenheit eine heparininduzierte Thrombozytopenie (HIT) vom Typ II aufgetreten ist.