GORE® VIABAHN® VBX ballonexpandierbare Endoprothese – Klinische Daten

Nachweislicher klinischer und Implantationserfolg*
≤ 30 % Reststenose aufgrund der hohen Radialkraft, selbst bei stark kalzifizierten und nicht-elastischen Läsionen.
Wiederherstellung des Lumendurchmessers1
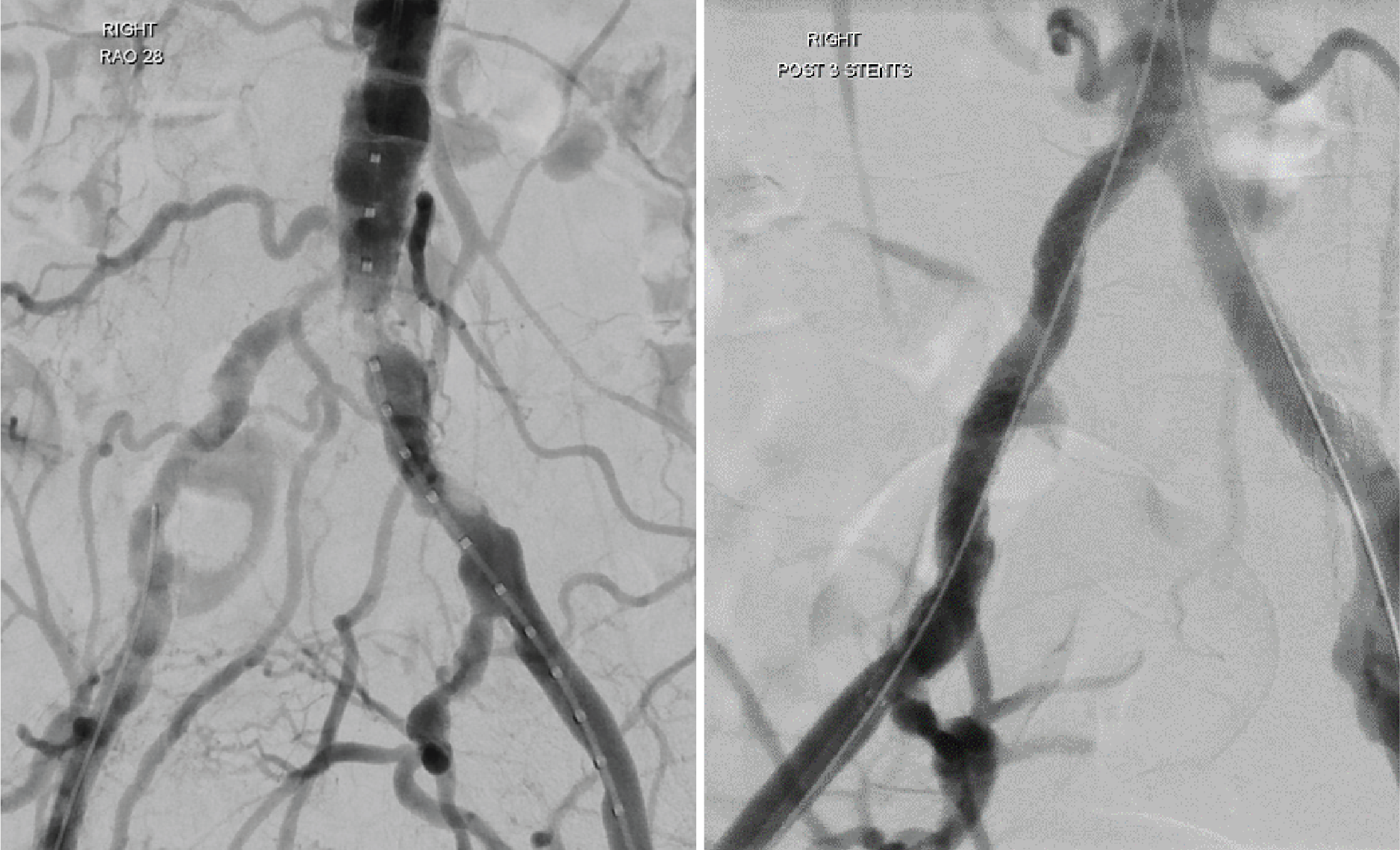
Bei der klinischen Gore VBX FLEX Studie handelt es sich um eine prospektive, multizentrische, einarmige Studie an 134 Patienten mit komplizierter aortoiliakaler Verschlusskrankheit (32,1 % TASC II C und D, 42,5 % Kissing-Stent).
In der Studie wurden 234 Produkte implantiert; 50 % bilaterale Behandlung, 18 % kontralaterale Implantation. Es war keine Vordilatation erforderlich.
Beibehaltung der Stentlänge*,1
Die mediane Längenänderung betrug 0 mm vor der Freisetzung des endgültigen Implantats
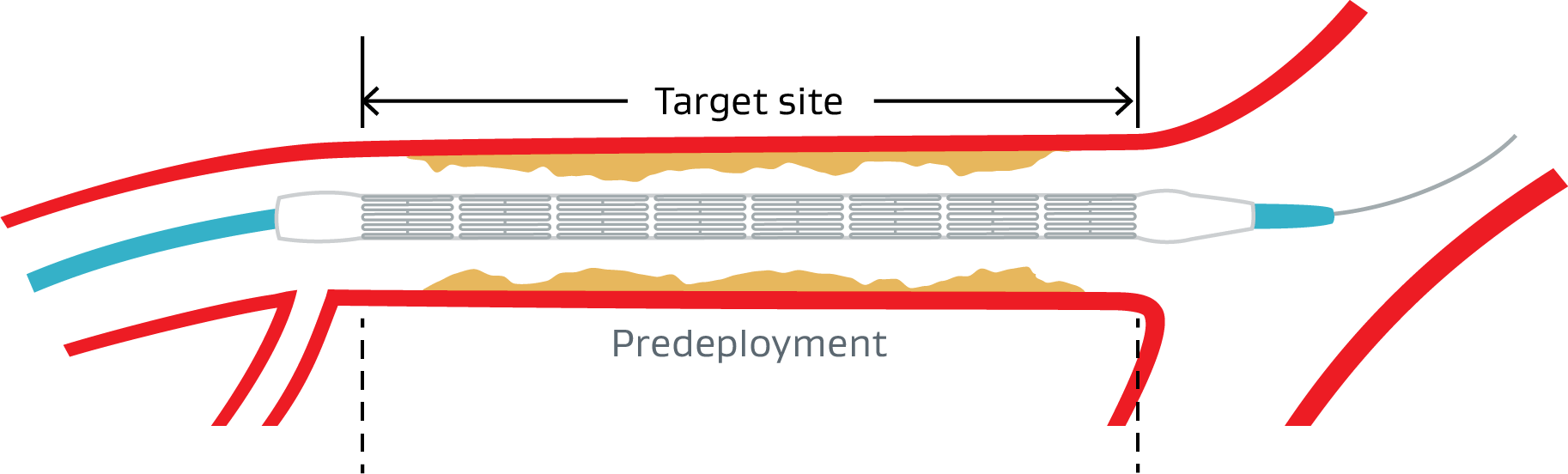

Stentfreisetzung*
- 100 % Freisetzung im Bereich der Zielläsion ohne Dislokation des Stents1
- 100 % Stentretention1
- 100 % Freisetzung am Zielort1
Nachgewiesene Offenheitsraten und Patientennutzen*
5-Jahres-Ergebnisse
Die Langlebigkeit der VBX Endoprothese wurde über einen Zeitraum von 5 Jahren in einer von Ärzten initiierten Studie untersucht, an der 59 Patienten aus 3 teilnehmenden Studienzentren teilnahmen, die repräsentativ für die Kohorte der VBX FLEX Studie sind.
Klinisch nachgewiesene Ergebnisse†,2
Primäre Offenheitsrate pro Läsion
Primär assistierte Offenheitsrate pro Läsion
fTLR pro Teilnehmer
Zusätzlicher Patientennutzen versus Baseline†,2
+0,15
Verbesserung beim mittleren ABI in Ruhe (von 0,76 bis 0,95) [p < 0,001]‡
3-fache
Verbesserung der mittleren Werte beim Walking Impairment Questionnaire (WIQ)
100 %
ausgewertete Patienten (n = 28) mit Verbesserungen ≥ 1 in der Rutherford-Klassifikation ab Baseline§
3-Jahres-Ergebnisse
91,2 %
Freiheit von Revaskularisierung der Zielläsion (fTLR)3
+0,17
Verbesserung beim mittleren Knöchel-Arm-Index (ABI) in Ruhe (p < 0,001, 0,93 mittlerer ABI)‡,3
92 %
Patienten mit Verbesserungen ≥ 1 in der Rutherford-Klassifikation versus Baseline3
1-Jahres-Ergebnisse
94,5 %
Primäre Offenheitsrate3
96,1 %
Primäre Offenheitsrate bei TASC-C- & -D-Läsionen nach 1 Jahr3
99,5 %
Sekundäre Offenheitsrate3
Publikationen
Ihre Quelle für aktuelle Publikationen und klinische Daten, die den Nutzen der GORE® VIABAHN® VBX ballonexpandierbaren Endoprothese in der Praxis belegen.
* Basierend auf früheren klinischen Daten. Aktuelle Neubewertung des Stentsystems mit verringertem Profil.
† Bei Indikationen und Konfigurationen von gecoverten Stents.
‡ (P < 0,001) Statistisch signifikante Veränderung zum Zustand vor dem Eingriff.
§ Es gab 59 Studienteilnehmer, und 28 Teilnehmer waren bis zum Studienende und danach für das 5-Jahres-Follow-up verfügbar.
- Bismuth J, Gray BH, Holden A, et al; VBX FLEX Study Investigators. Pivotal study of a next-generation balloon-expandable stent-graft for treatment of iliac occlusive disease. Journal of Endovascular Therapy 2017;24(5):629-637. http://journals.sagepub.com/doi/full/10.1177/1526602817720463
- Holden A, Takele E, Hill A, et al. Long-Term Follow-up of Subjects With Iliac Occlusive Disease Treated With the Viabahn VBX Balloon-Expandable Endoprosthesis. Journal of Endovascular Therapy. 2023;0(0). doi:10.1177/15266028231165723
- Panneton JM, Bismuth J, Gray BH, Holden A. Three-year follow-up of patients with iliac occlusive disease treated with the Viabahn Balloon-Expandable Endoprosthesis. Journal of Endovascular Therapy 2020;27(5):728-736. https://journals.sagepub.com/doi/10.1177/1526602820920569

Eine vollständige Beschreibung aller geltenden Indikationen, Warnhinweise, Vorsichtsmaßnahmen und Kontraindikationen für die Länder, in denen dieses Produkt angeboten wird, finden Sie in der Gebrauchsanweisung unter eifu.goremedical.com. RXOnly
INDIKATIONEN IN EUROPA: Die GORE® VIABAHN® VBX ballonexpandierbare Endoprothese ist zur Behandlung in den folgenden Fällen indiziert:
- De-novo-Läsionen oder restenotische Läsionen der Iliakalarterien, einschließlich Läsionen an der Aortenbifurkation;
- De-novo-Läsionen oder restenotische Läsionen der Viszeralarterien;
- Isolierte Aneurysmen der Viszeralarterien, Iliakalarterien und Subklaviaarterien;
- Traumatische oder iatrogene Gefäßschädigungen von Arterien, die sich in der Brusthöhle, im Bauchraum oder im Becken befinden (außer Aorta, Koronararterien, Truncus brachiocephalicus, Karotis, A. Vertebralis- und A. Pulmonalis).
Die GORE® VIABAHN® VBX ballonexpandierbare Endoprothese ist zur Verwendung als Bridging Stent bei Behandlungen von gebranchten und fenestrierten endovaskulären Aortenaneurysmen mit den folgenden Produkten indiziertII:
- Zugelassene gebranchte endovaskuläre Aortenprothesen, bestehend aus Polyestergewebe, Edelstahlstents und Polypropylen-Nahtmaterial, wobei die Branchkomponenten einen Durchmesser von 6/8 mm und eine Länge von 18/21 mm aufweisen.
- Zugelassene fenestrierte endovaskuläre Aortenprothesen, bestehend aus Polyestergewebe, Edelstahlstents und Fenestrationen aus Polypropylen-Nahtmaterial, wobei der Durchmesserbereich bei 6–8 mm liegt.
KONTRAINDIKATIONEN: Die GORE® VIABAHN® VBX ballonexpandierbare Endoprothese darf bei Patienten mit bekannter Überempfindlichkeit gegen Heparin nicht angewendet werden. Dies gilt insbesondere auch für die Patienten, bei denen in der Vergangenheit eine heparininduzierte Thrombozytopenie (HIT) vom Typ II aufgetreten ist.
II Nicht zutreffend für die GORE® VIABAHN® VBX ballonexpandierbare Endoprothese mit verringertem Profil (BXB-Bestellnummern).